1. 서 론
2. 재료 및 방법
담치 사육 및 미세플라스틱
미세플라스틱 노출 실험
MP 체내 축적량 분석
담치 조직 샘플링 및 TUNEL분석
담치 RNA 추출 및 p53 유전자발현 분석
통계적 분석
3. 결과 및 고찰
MP 노출에 따른 지중해담치 체내축적
MP 노출에 따른 지중해담치 조직 세포독성
MP 노출에 따른 지중해담치 p53 유전자 발현
4. 결 론
1. 서 론
플라스틱의 대량 생산으로 2050년까지 생산량이 330억 톤에 이를 것으로 예상된다(Covernton et al. 2022). 이로 인해 해양 생태계에서 플라스틱은 보편적으로 발견되며 지배적으로 서식환경에 영향을 주고 있다(Cole et al. 2011; Xu et al. 2020; Rellán et al. 2023). 플라스틱은 환경에서 파편화 되어 직경 5 mm 미만의 입자인 미세플라스틱(MP)을 생성한다. 해양 환경의 MP 오염은 전 세계적으로 생물 유해성에 대한 관심이 나날이 커지고 있다. 먹이망을 통한 MP 섭취 및 이동은 다양한 생물 종에게 독성 영향을 미칠 수 있어 MP를 잠재적 독성물질로 간주하고 있으며, 플라스틱 제품 가공과정에서 첨가되는 화학물질로 인해 MP 노출에 따른 해양생물의 생존에 대한 위협이 발생하고 있다. 또한 환경에 존재하는 동안 축적될 수 있는 잔류성 유기 오염물질이다(Sharifinia et al. 2020). 수환경에서 발견되는 MP는 다양한 형태(섬유, 파편, 필름 등), 구성 화학성분(폴리에틸렌 테레프탈레이트(PET), 폴리스티렌(PS), 폴리염화비닐(PVC) 등), 입자 크기와 농도에 따라 해양환경내 분포 뿐 아니라 다양한 서식 해양생물 군에서 유해물질로서의 위험성이 보고되고 있다(Xu et al. 2020; Fagiano et al. 2023; Osman et al. 2023).
작은 무척추동물부터 큰 척추동물까지 광범위한 해양 생물은 다양한 환경 조건에서 생존에 영향을 미치는 MP 섭취에 취약하다(Guzzetti et al. 2018). MP 노출은 어류의 소화관, 아가미, 피부를 통해 체내로 유입되어 산화적 스트레스 유발을 통한 조직 손상이나 생식 기관의 기능에 부정적 영향을 미친다(Liu et al. 2024). 망둥어(Pomatoschistus microps) 치어에서 MP 노출은 산화적 손상과 함께 아세틸콜린에스테라제(AChE) 활성의 감소가 나타났다(Oliveira et al. 2013). 저서생물 중 다모류인 갯지렁이(Arenicola marina)는 MP 노출 스트레스로 건강상태 뿐 아니라 섭식 및 퇴적물 여과 행동에도 부정적인 영향이 나타났다(Pires et al. 2022). 고농도의 MP 노출은 이매패류에서 면역기능의 이상과 생리적 스트레스로 인한 치사율의 증가도 나타났다(Browne et al. 2008; Green 2016). 또한 고밀도 폴리에틸렌(HDPE)의 장기 노출은 유럽굴(Ostrea edulis)의 호흡 및 여과율을 증가시켰다(Green 2016; Green et al. 2017).
해양 저서생물, 특히 Mytilus edulis L. 및 Mytilus galloprovincialis (Lamarck 1819) 종과 같은 Mytilus 속의 담치는 수생 환경의 건강 상태를 평가하고 해양 오염을 모니터링하기 위한 생물지표로 이용된다(Capillo et al. 2018; Hellfeld et al. 2022; Park et al. 2024). 지중해담치(Mytilus galloprovincialis)는 거의 모든 해안선에서 발견되며 전 세계적으로 해안의 바위나 모래 바닥 지대에 서식하는 보편적인 이매패류이다(Chelyadina et al. 2022; Oyarzún et al. 2024). 담치는 고착성 생활 방식을 갖고 있으며, 많은 양의 물을 여과하고, 일반적으로 견딜 수 있는 다양한 해양 오염 물질을 섭취하여 조직에 축적할 수 있는 특성이 있다. 담치 체내 오염 물질의 축적은 산화 스트레스를 증가시켜 궁극적으로 세포손상과 연결될 수 있다 (Matozzo et al. 2016). 해양 환경오염 물질에 대한 이매패류의 안전성은 해양환경 모니터링 뿐 아니라 수산물 섭취로 인한 인간의 건강성과 밀접하게 관련된다. MP의 섭취는 담치의 입쪽에서 이동하여 소화선으로 들어가거나 생식선 조직까지 도달하여 발견된다(Von Moos et al. 2012; Fernández and Albentosa 2019; Cui et al. 2021). MP 입자의 이매패류 내 체류시간이 길수록 소비 시 다음 영양 수준으로 옮겨질 가능성이 높을 뿐만 아니라 화학 물질 및 기타 화합물이 입자에서 잠재적으로 탈착되는데 더 많은 시간이 걸리기에 독성 영향이 증폭될 수 있다(Avio et al. 2015; Koelmans et al. 2016). 이에 이매패류인 담치에서 MP의 잠재적 독성 연구는 매우 중요하다. 하지만 MP 노출에 따른 이매패류의 생리적 반응 외에 세포수준에서의 노출독성 영향에 대한 연구는 제한적이다.
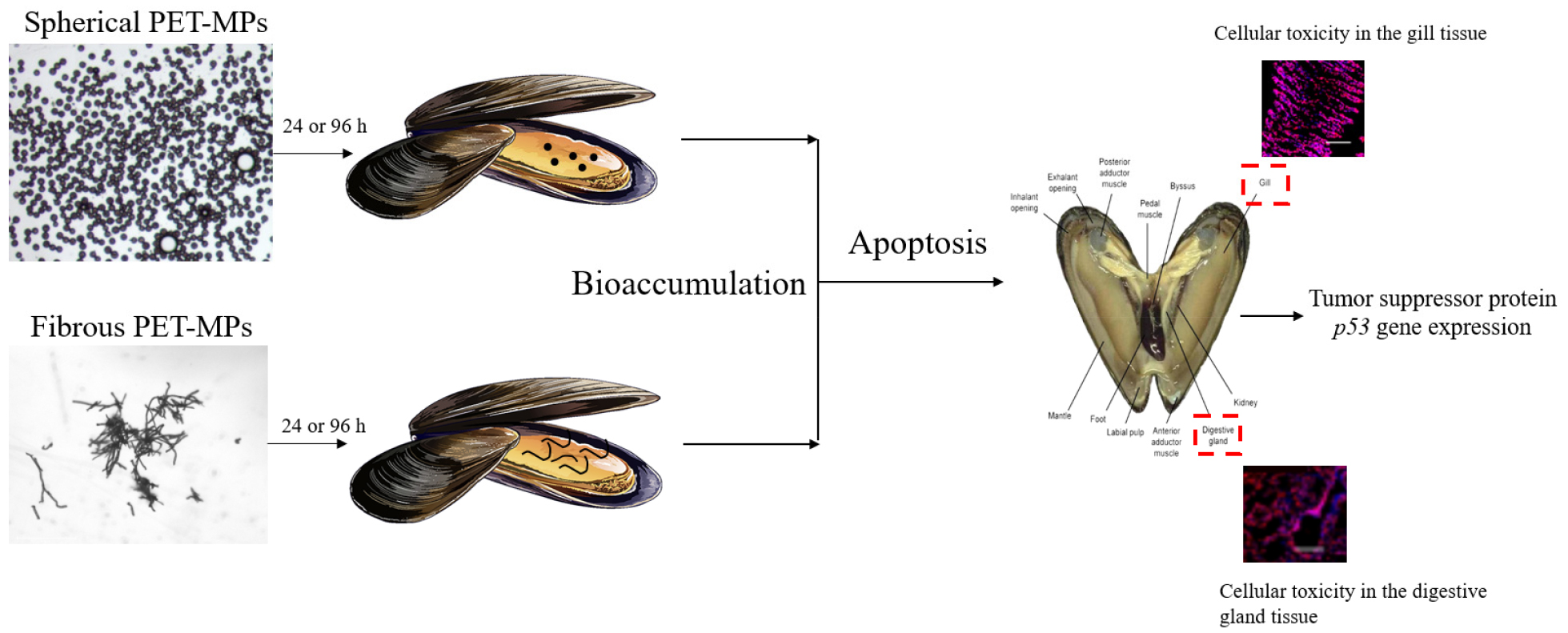
이에 본 연구에서 MP 형태에 따른 이매패류 노출 세포독성을 조사하기 위해, 구형(spherical)과 섬유형(fibrous) MP 급성 노출에 따른 지중해담치(M. galloprovincialis)의 체내축적과 조직별(아가미와 소화선 조직) 세포반응을 관찰하였다. 나아가 MP 노출에 따른 세포사멸(apoptosis)관련 유전자인 p53 유전자의 발현패턴 분석을 통해 MP의 세포독성을 확인하였다. MP 형태(구형, 섬유형)에 따른 지중해담치의 체내축적의 차이가 조직 손상 및 세포사멸 반응 유도에 잠재적 독성 차이를 유도하는지 분석하였다.
2. 재료 및 방법
담치 사육 및 미세플라스틱
지중해담치(M. galloprovincialis)는 평균 길이 4.5 ± 0.5 cm로 2022년 6월 여수 양식장 시장(N34°44′45.5424″ N, 127°39′17.6472″ E)에서 구입하여 사용하였다. 실험실로 이동한 담치들은 인공해수(ASW, 25‰ salinity with commercial sea salts (Aquaforest® Sea Salt, Poland))가 포함된 3.7 L (지중해담치 약10 마리) 수조에서 일정한 환경조건(20 ± 1°C, pH 7.5 ± 0.5, 염도 25 ± 0.5‰, 평균 ± 표준편차)에서 사육되었다. 실험 전 7일 동안 순치하였으며 용존산소(DO)는 80% 이상의 포화도를 유지하였다. 수질환경은YSI 수질 모니터링 측정기(ProQuatro, a xylem brand)를 이용해 측정하며 매일 체크하였다. 제공되는 먹이는 두가지 혼합 상업용 사료인 미세조류 사료(0.3 mL per mussel; 0.1 mL of Nanno 3600 and 0.2 mL of Shellfish Diet 1800TM, Reed Mariculture, Campbell, CA, USA)를 매일 공급하였다. 본 연구에서 노출 실험에 사용한 MPs는 Cospheric LLC에서 구입한 구형 PE MP (Cospheric Microspheres PMS-BG-1.00 27–32 μm)와 한국생산기술연구원(KITECH, Ansan, Korea)에서 공급받은 폴리에틸렌 테레프탈레이트(PET: polyester 100%)의 섬유형 MP (200–400 μm: 직경 12.95 ± 0.91 μm)이다. MP의 표면과 조성은 주사전자현미경(HR FESEM SU8010; Hitachi, Tokyo, Japan)과 532 및 785 nm 레이저를 사용하는 라만 현미경(RAMANtouch, Nanophoton, Osaka, Japan)으로 확인하였다.
미세플라스틱 노출 실험
미세플라스틱 노출 실험은 대조군(ASW)과 구형 MP (27–32 μm) 및 섬유형 MP (200–400 μm)의 3개 실험 그룹으로 구분된다. 지중해담치는 1, 10, 100 mg L-1 MPs 농도에서 24시간과 96시간 동안 노출되었고(Park et al. 2024), 각 실험 그룹은 5개의 반복 탱크로 구성되었다. 각 탱크에는 3.7 L의 실험수에 10 마리의 담치 개체가 포함되고 실험기간동안 실험수는 각 MP가 포함된 해당 양의 배지로 완전히 교환되었다. 노출 실험 환경 조건은 사육 환경과 동일한 조건으로 진행하였다.
MP 체내 축적량 분석
지중해담치 체내 MP 축적량 분석은 노출 24와 96시간에 담치 샘플을 준비하여 Park et al. (2024)의 조직 소화법을 통한 MP 개수 분석방법으로 수행하였다. 담치 조직의 무게는 측정하여 wet/dry로 나타내고, 각 MP 당 노출 시간에 따라 10마리의 지중해 담치를 분석하였다. 담치 조직이 담긴 튜브에 10% KOH 20 mL를 첨가하고 샘플을 40°C에서 72시간 동안 배양하여 조직을 녹인다. 포화 NaI 용액 10 mL로 세 번 헹구어 MP를 분리하고, MP가 포함된 현탁액을 0.7 μm 유리 microfiber 필터(47 mm, Whatman, UK)로 여과하여 광학 현미경을 사용하여 MP 수를 계산하였다. 담치내 흡수된 섬유형 MP를 시각화하기 위해 나일 레드(Sigma-Aldrich, Saint Louis, MO, USA)로 형광 염색하고, 형광 표지된 구형 MP는 EVOS™ FL Auto 2 이미징 시스템(Invitrogen, Thermo Fisher Scientific, MA, USA)으로 관찰하였다.
담치 조직 샘플링 및 TUNEL분석
지중해담치는 분석을 위해 24시간과 96시간에 샘플링 하여, 각 실험 탱크에서 6개의 담치를 채취하여 조직을 분리했다. 조직을 PBS로 세척한 후 파라핀화 하기전 4°C에서 4% (v/v) 파라포름알데히드(PFA)에 24시간 고정하거나 RNA 추출까지 -80°C에서 보관하였다. 고정된 조직은 조직 처리기와 파라핀 포매 기계(Leica, IL, USA)를 사용하여 파라핀 블록을 만들었다. 회전식 마이크로톰(Roundfin RD-315, Shenyang, China)을 사용하여 4 μm 섹션 간격으로 잘라 유리 슬라이스에 옮겼다. 염색 전, 일련의 자일렌, 자일렌:100% 에탄올(1:1 비율, v/v), 100%, 95%, 80% 에탄올 및 DW를 사용하여 순서대로 파라핀 제거(deparafinization)와 재수화(rehydration)를 진행하였다. Apoptosis 관찰을 위한 TUNEL 분석은 제조업체의 프로토콜에 따라 One-step TUNEL In Situ Apoptosis Kit (Elabscience, Texas, USA)를 이용하여 수행하였다.
담치 RNA 추출 및 p53 유전자발현 분석
지중해담치 RNA는 제조사의 프로토콜에 따라 TRIzol 시약(Invitrogen, CA, USA)을 사용하여 아가미와 소화선 조직에서(약 35 mg crab-1) total RNA를 추출하였다. Recombinant DNase I (RNase-free) (Takara, Kusatsu, Japan)을 사용하여 추출된 RNA에서 genomic DNA를 제거하였다. RNA 농도는 Nano-Drop 1000 system (Thermo Fisher Scientific, Waltham, MA, USA)을 이용하여 측정하였고, 농도 조절을 위해 nuclease-free water (Invitrogen, Waltham, MA, USA)를 사용하였다. RNA integrity는 1% 아가로스 젤 전기영동을 통해 확인하고 샘플은 -80°C에 보관하였다. cDNA합성은 total RNA에서 iScript Reverse Transcription Supermix (1708841, Bio-Rad, CA, USA)를 이용하여 수행하였다.
Quantitative real-time reverse transcription PCR (qRT- PCR)을 통해 대조군과 각각의 MP 노출 처리군에서 p53 유전자의 mRNA 발현 수준을 실시간 정량적으로 측정하였다. qRT-PCR은 AccuPowerR 2x GreenStarTM qPCR Master Mix (Bioneer, Daejeon, Korea)를 사용하여 수행하였다. PCR mixture는 30배 희석한 cDNA 5 μL, 2x SYBR 10 μL, 각 프라이머(10μM) 0.5 μL 및 DEPC-treated water를 포함하여 총 20μL로 하였으며, PCR cycle조건은 다음과 같다: 95°C에서 2분, 95°C에서 15초, 60°C에서 20초, 72°C에서 1분의 40회 반복. Beta-actin (β-actin) 유전자는 상대 발현 분석을 위한 대조군으로 이용하였다. 각 샘플은 3번 반복하여 반응을 수행하였다. 상대적인 유전자 발현 수준은 2-ΔΔct 방법으로 대조군 유전자인 β-actin 발현양에 대한 CT 값으로 정규화하여 분석하였다. p53 유전자(KC545827)의 프라이머 시컨스는 forward: 5’-AGATCCATATACCAGCCGC C-3’, reverse: 5’-CTA CTGCCCGTCTACCTAGC-3’로 PCR product 사이즈는 188bp이다. β-actin 프라이머 시컨스는 forward: 5′-CGG TACCACCATGTTCTCA G-3′이고 reverse: 5′-GACCGG ATTCATCGTATTCC-3′ (Toubiana et al. 2013).
통계적 분석
구형과 섬유형 MP 노출에 따른 체내축적 및 p53 유전자 발현의 변화를 통계적으로 비교하기 위해 R 프로그램(ver 4.3.1, RS Team, Inc., Boston, MA, USA)을 사용하여 t-test를 수행하였다. 최소 3번의 독립적인 실험(n = 3)에서 얻은 데이터를 평균화하고 평균 ± 표준편차로 표시하였다. 통계적으로 유의한 차이는 0.05 미만의 p-값으로 제시하였다(*p < 0.05).
3. 결과 및 고찰
MP 노출에 따른 지중해담치 체내축적
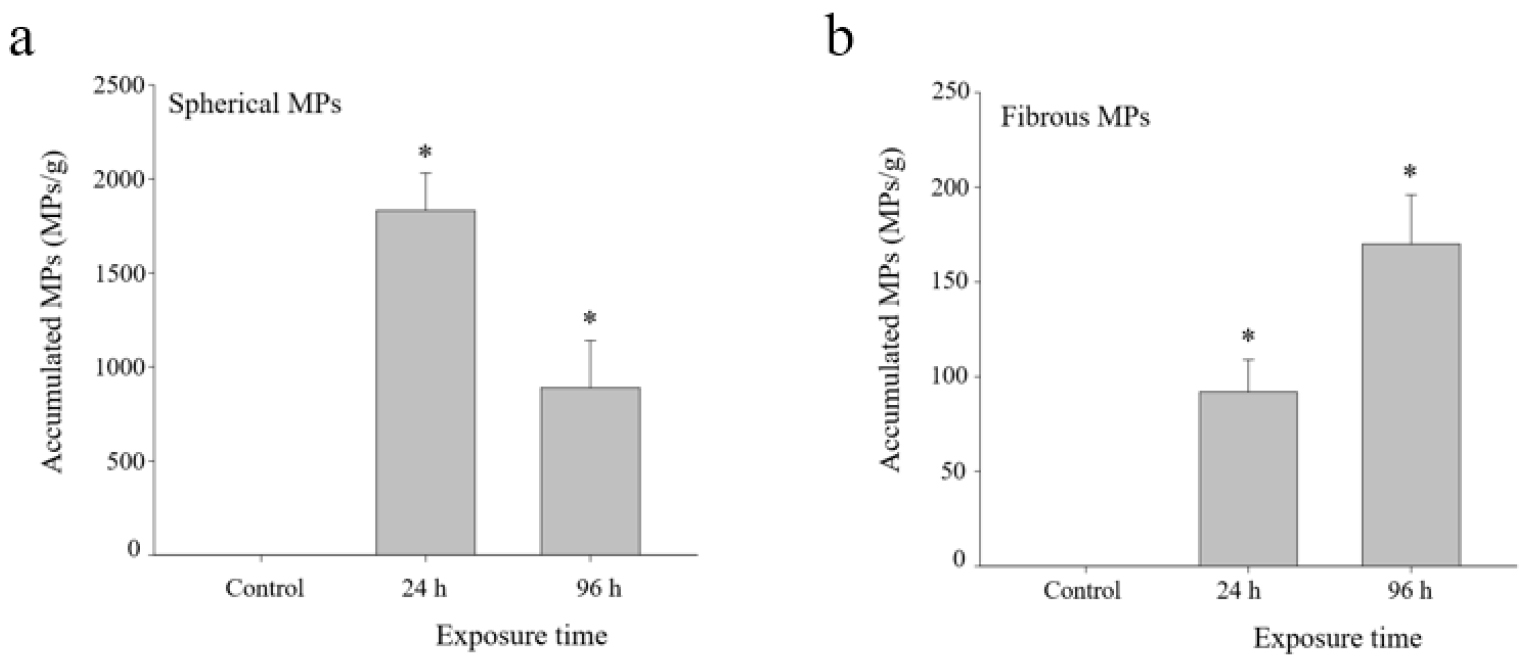
지중해담치의 구형과 섬유형 MP 노출후 24시간과 96시간에 Whole body에서 관찰하였다(Fig. 1). 구형 MP 노출시 대조군에 비해 24시간에는 높은 체내축적이 확인되었다(Fig. 2a). 하지만 노출 96시간에는 상대적으로 감소된 체내축적이 관찰되지만 대조군에 비해 구형 MP 노출시 통계적으로 유의한 수준의 체내축적 증가를 확인하였다(p < 0.05). 섬유형 MP는 노출 시간이 지남에 따라 더 높은 축적이 관찰되는데, 24시간 보다 96시간에 섬유형 MP 체내축적이 증가되어 대조군에 비해 통계적으로 유의한 수준(p < 0.05)으로 확인되었다(Fig. 2b). 지중해담치에서 전체적인 MP의 체내 축적량은 구형이 섬유형에 비해 높게 나타났다. 담치와 같은 연체동물은 다양한 수환경에서 풍부하게 분포하고 고착성 및 여과 섭식의 생리적 특성과 생태적-경제적 가치가 있어 환경오염 물질의 독성 및 생물축적에 주요한 생물 지표로, MP 노출에 따른 민감한 축적 반응이 나타난다(Woolnough et al. 2020; Park et al. 2024; Blasco et al. 2024). MP는 다양한 농도로 아가미, 근육, 소화선에 축적된다고 보고된다(Sendra et al. 2020). 지중해담치는 수층에서 MP를 섭취하여 소화계에 축적할 수 있으며 아가미 조직내의 축적 효율은 입자의 크기에 따라 달라진다(Blasco et al. 2024). MP의 형태와 크기는 지중해담치의 섭취에 따른 체내축적 차이가 나타난다. 노출시간에 따라 작은 크기의 구형 MP는 노출 초기에 급격히 축적되며 섬유형 MP는 오히려 노출시간 의존적으로 서서히 축적되는 것을 확인하였다(Park et al. 2024). 이러한 체내축적의 패턴은 담치의 체내배출과 연관되어 궁극적인 독성영향을 일으키는 주요한 원인이 된다. 구형 MP가 체내축적이 빠르게 많이 되지만 배출도 빠르기에 노출시간에 따라 축적량의 감소가 나타나고, 섬유형 MP의 체내축적은 구형 MP에 비해 느려서 축적량이 낮지만 실타래 모양으로 체내에서 엉켜서 배출이 용이하지 않아 노출시간에 따라 축적량의 증가가 관찰되는 것으로 제시된다. 지중해담치의 MP 체내축적은 해양 생태계의 모니터링 뿐 아니라 수산물섭취에 있어 인간 건강성에도 직접적으로 부정적 영향을 유도하게 된다.
MP 노출에 따른 지중해담치 조직 세포독성
구형과 섬유형 MP의 형태에 따른 지중해담치의 조직별 세포독성은 TUNEL assay를 통해 관찰하였다(Figs. 3, 4, 5, 6). 지중해담치 아가미(gill) 조직에서 구형과 섬유형 MPs 24시간 노출 결과, 구형과 섬유형 MP의 상대적으로 고농도인 100 mg L-1에서 세포독성이 증가하는 경향이 나타났다(Fig. 3g and h). 노출 24시간에는 구형이 섬유형 MP에 비해 상대적으로 더 높은 세포독성이 관찰된다. 하지만 96시간 MP 노출된 아가미 조직에서는 섬유형 MP가 노출 농도 의존적으로 세포독성이 증가하였다(Fig. 4). 구형 MP에 96시간 노출된 아가미조직 세포독성은 상대적으로 저농도인 1 mg L-1에서는 관찰되지 않았고 고농도에서는 대조군에 비해 뚜렷하게 증가하는 것이 확인되었다(Fig. 4c, e and g). 섬유형 MP에 96시간 노출된 아가미 세포독성은 저농도에서도 나타났으며 고농도에서는 positive 대조군의 50% 이상으로 증가하여 높은 세포독성이 확인되었다(Fig. 4d, f and h). 지중해담치의 소화선 조직(digestive gland)에서의 세포독성은 구형과 섬유형 MPs 노출 24시간에 대조군과 유사하게 나타났다(Fig. 5). 또한 96시간 노출에서 구형 MP의 상대적 고농도에서는 세포독성이 나타나기 시작하지만(Fig. 6g), 구형과 섬유형 MPs 노출에 따른 세포독성 증가는 소화선 조직에서 뚜렷하게 관찰되지 않았다. MP 노출에 따른 조직 세포독성은 소화선 조직 보다 아가미 조직에서 더 민감하게 나타났으며 노출농도 의존적인 증가가 확인되었다. 상대적으로 고농도의 MP 노출에서 24시간에는 구형 MP가 96시간에는 섬유형 MP가 더 높은 아가미 세포독성 증가를 유도하였다(Figs. 3 and 4). 본 연구에서 MP 노출에 따른 세포독성의 증가는 노출 조직 및 시간과 MP 형태에 따라 다르게 관찰되었다. 이러한 세포독성의 증가는 MP노출에 따른 DNA fragmentation의 증가와 연관된다(Mai et al. 2023). 아가미 조직은 외부 오염물질의 섭취에 가장 가까이 접촉하고 있는 부분으로 호흡 및 물질 여과-확산에 주요한 기능을 한다(Kim et al. 2024). 구형과 섬유형 MP의 노출은 소화기능을 담당하는 소화선 보다 물질 여과에 필수적인 아가미 조직에서 높은 세포독성이 나타남으로 아가미 조직내 DNA damage가 발생함을 제시한다. MP를 섭취하면 해양생물의 위장관 생리가 변화하고, 세포독성 증가, 면역 체계 저하, 산화 스트레스 생성 및 항산화 관련 유전자 발현 차이가 생겨 결과적으로 성장 억제를 유도한다는 결과가 보고되었다(Osman et al. 2023). 구형 MP는 노출 초기에 급격히 체내축적이 증가하고 시간이 지날수록 감소하지만, 섬유형 MP의 시간 의존적인 체내축적 증가는 DNA damage 생성으로 유도되는 세포사멸과 궁극적으로 연결된다. 나아가 polymer 종류가 다른 MP 노출에 따른 세포독성 유도의 반응도 추후에 확인되어야 한다.
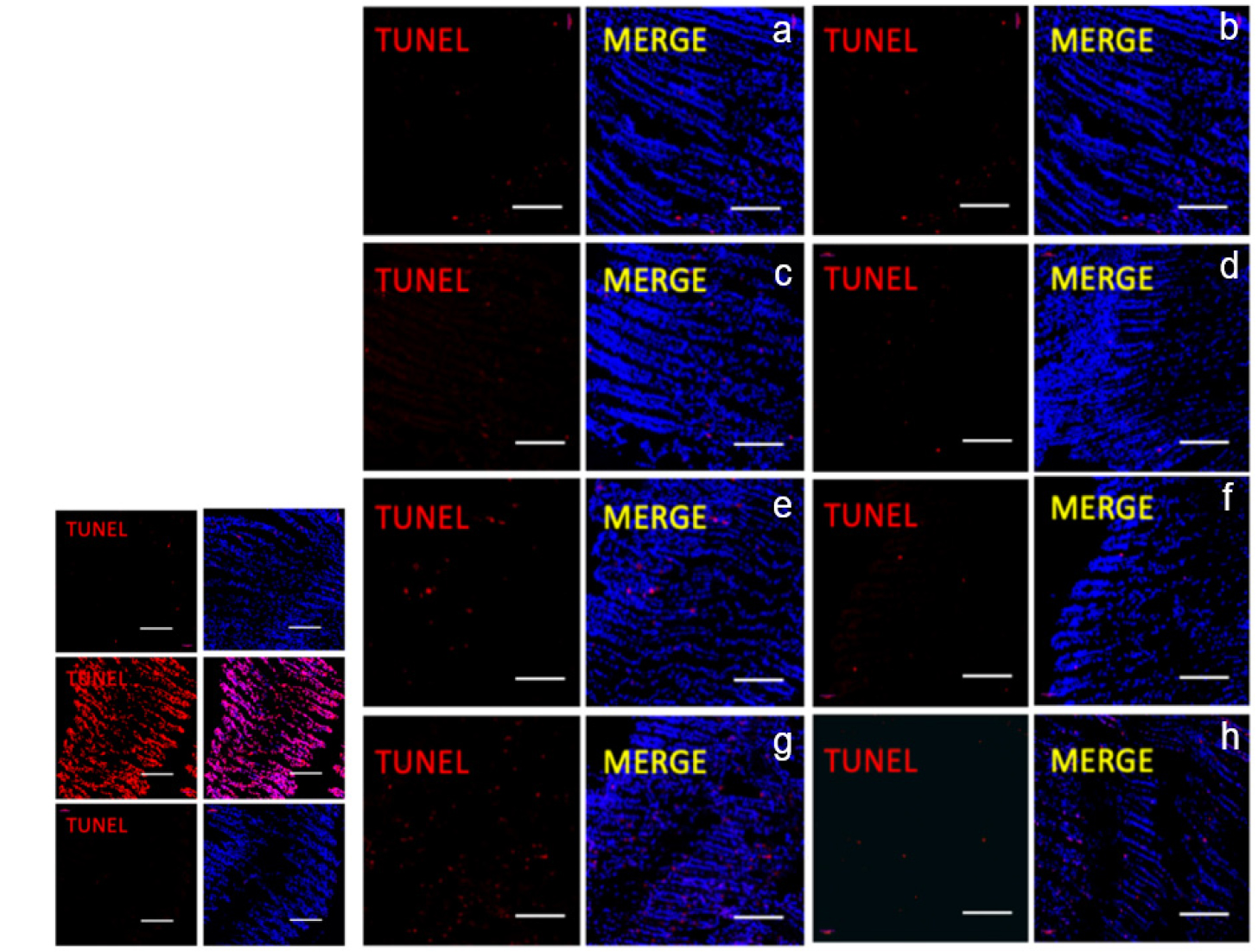
Fig. 3.
Cell apoptosis observation on the gill of Mytilus galloprovincialis exposed to spherical (a, c, e, g) and fibrous (b, d, f, h) MPs for 24 h using TUNEL assay. a and b: control, c and d: 1 mg L-1, e and f: 10 mg L-1, and g and h: 100 mg L-1. Red cells were indicated as cell with DNA damage. Scale bar, 100 μm
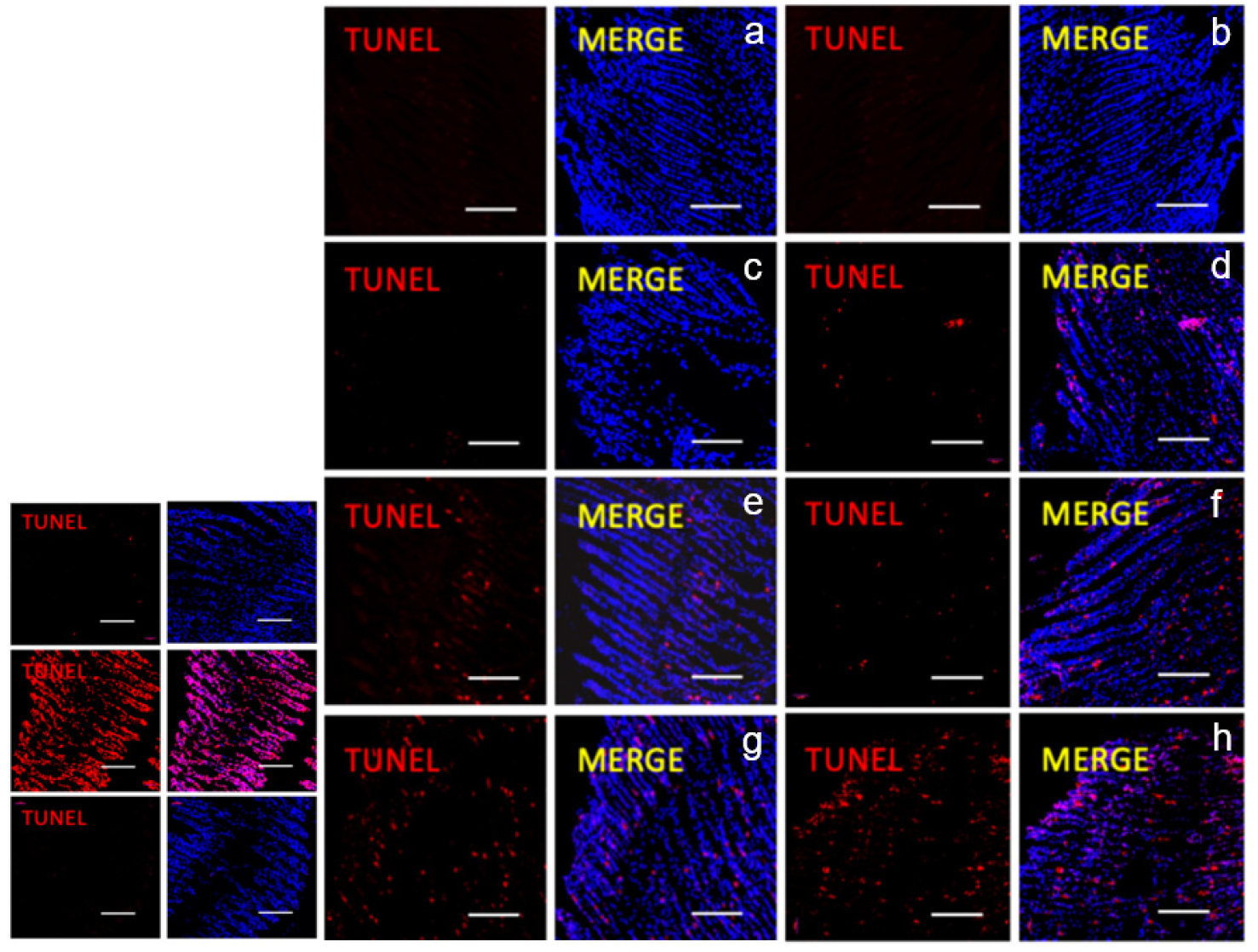
Fig. 4.
Cell apoptosis observation on the gill of Mytilus galloprovincialis exposed to spherical (a, c, e, g) and fibrous (b, d, f, h) MPs for 96 h using TUNEL assay. a and b: control, c and d: 1 mg L-1, e and f: 10 mg L-1, and g and h: 100 mg L-1. Red cells were indicated as cell with DNA damage. Scale bar, 100 μm
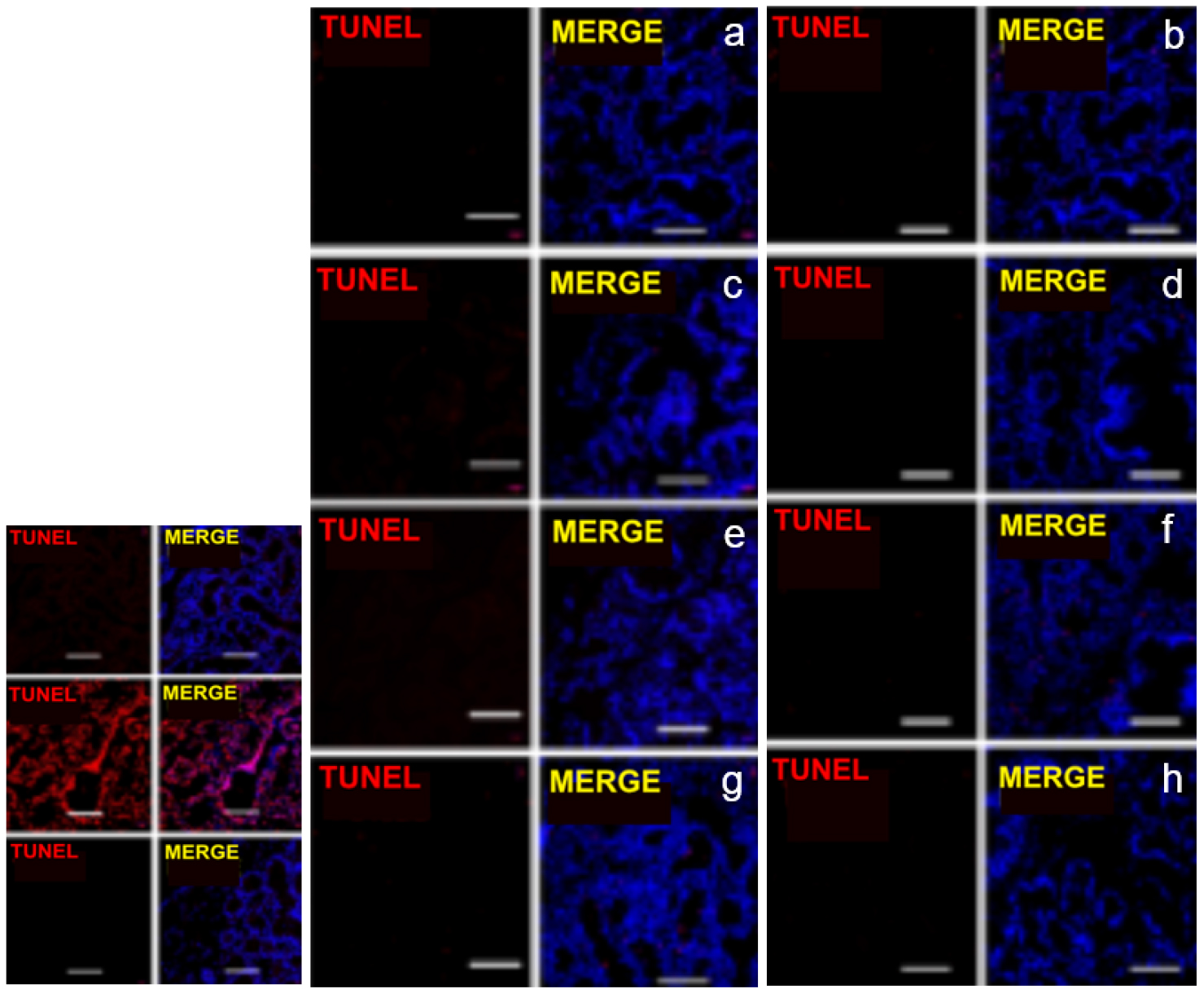
Fig. 5.
Cell apoptosis observation on the digestive gland of Mytilus galloprovincialis exposed to spherical (a, c, e, g) and fibrous (b, d, f, h) MPs for 24 h using TUNEL assay. a and b: control, c and d: 1 mg L-1, e and f: 10 mg L-1, and g and h: 100 mg L-1. Red cells were indicated as cell with DNA damage. Scale bar, 100 μm
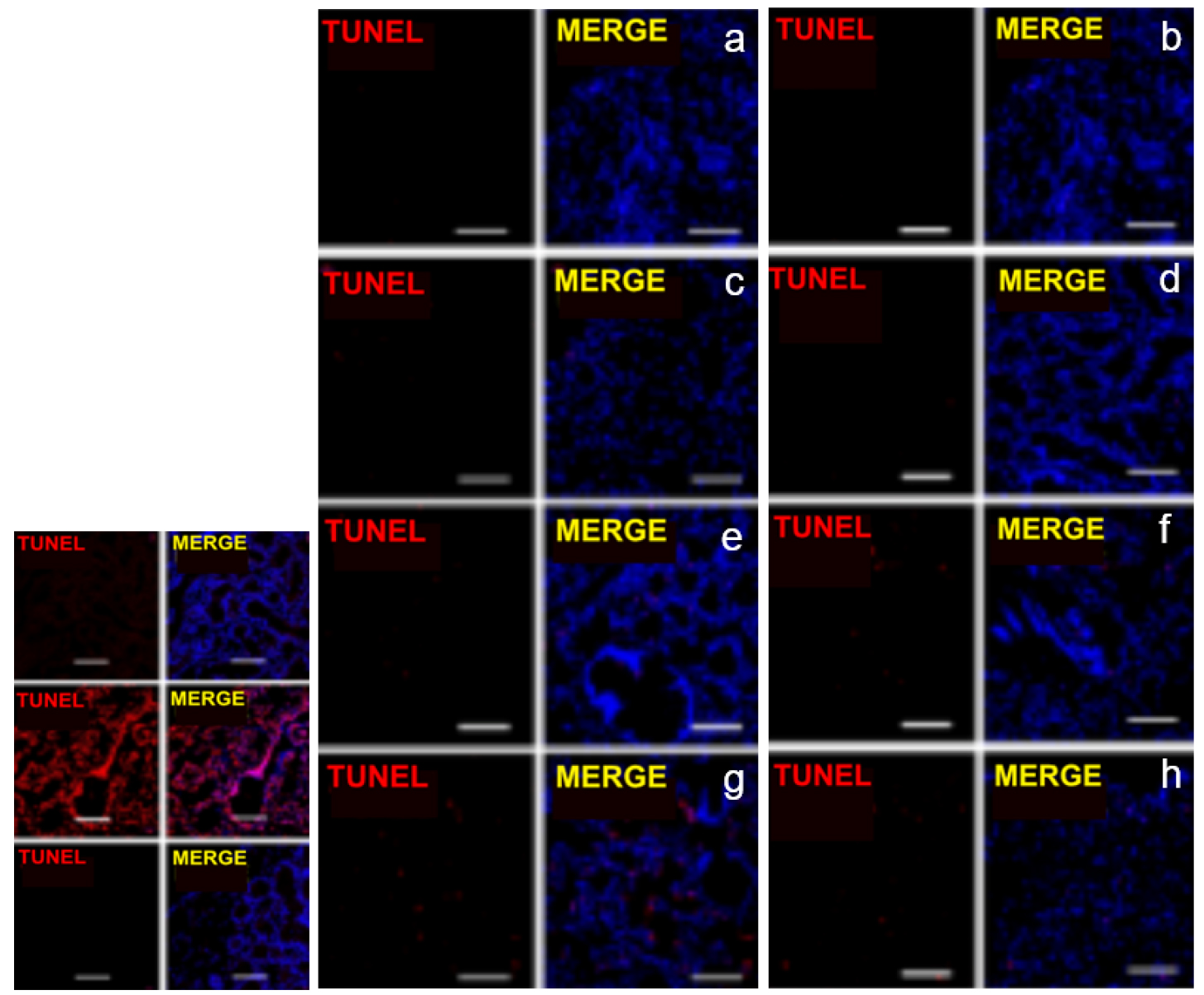
Fig. 6.
Cell apoptosis observation on the digestive gland of Mytilus galloprovincialis exposed to spherical (a, c, e, g) and fibrous (b, d, f, h) MPs for 96 h using TUNEL assay. a and b: control, c and d: 1 mg L-1, e and f: 10 mg L-1, and g and h: 100 mg L-1. Red cells were indicated as cell with DNA damage. Scale bar, 100 μm
MP 노출에 따른 지중해담치 p53 유전자 발현
지중해담치에서 구형과 섬유형 MP 노출에 따른 세포사멸 관련 유전자인 p53의 발현 패턴을 분석하였다(Fig. 7). 아가미 조직에서 p53 유전자는 구형과 섬유형 MP 노출에 따라 통계적으로 유의한 수준으로(p < 0.05) 발현이 증가하였다. 노출 24시간에는 구형 MP가 96시간에는 섬유형 MP에서 p53의 발현이 상대적으로 높게 나타났다. 지중해담치의 아가미 조직에서 가장 높은 p53 발현양은 섬유형 MP의 96시간 노출에서 확인되었다. 소화선 조직에서의 p53 유전자발현은 구형과 섬유형 조직에서 대조군에 비해 통계적 유의한 수준으로 증가하지 않았다(p > 0.05). 암을 억제하는 단백질인 p53 유전자는 세포주기조절, DNA 복구, 세포사멸, 세포 노화 등의 과정에 관여한다(Hou and Yang 2013; Park and Kwak 2022). 이러한 p53 유전자의 기능은 DNA fragmentation을 막아 게놈의 안정화에 중요한 역할을 하기에, MP 노출에 따른 p53 발현 변화는 DNA damage 유도를 통한 세포사멸의 진행과 연결된다(Zhang et al. 2013; Rangaswamy et al. 2024). 지중해담치의 p53 유전자발현은 조직별 세포독성과 유사한 결과가 나타났다. 소화선 보다 아가미 조직에서 통계적으로 유의한 수준의 p53 발현 증가가 관찰되었고 이는 MP 노출로 인해 DNA damage 발생시키는 세포독성이 세포사멸을 유도하고 이는 궁극적으로 p53 유전자의 발현패턴 변화를 통한 기능이상과 관계된다. p53과 anti-apoptotic BCL2 유전자의 발현은 세포사멸 과정을 제어하고 세포 생존을 촉진하는 메카니즘의 핵심이다. 전사체(transcriptome) 분석은 섬유형 MP에 노출된 지중해담치가 p53과 BCL2 유전자의 조절을 통해 세포 생존 효과를 지연하는 것을 확인하였다(Rangaswamy et al. 2024). 또한 다른 형태의 MP 노출은 AKT 및 ERK 신호 전달 경로의 억제를 통해 지중해담치의 미토콘드리아 경로 매개 세포 사멸을 유도하였다(Mai et al. 2023).
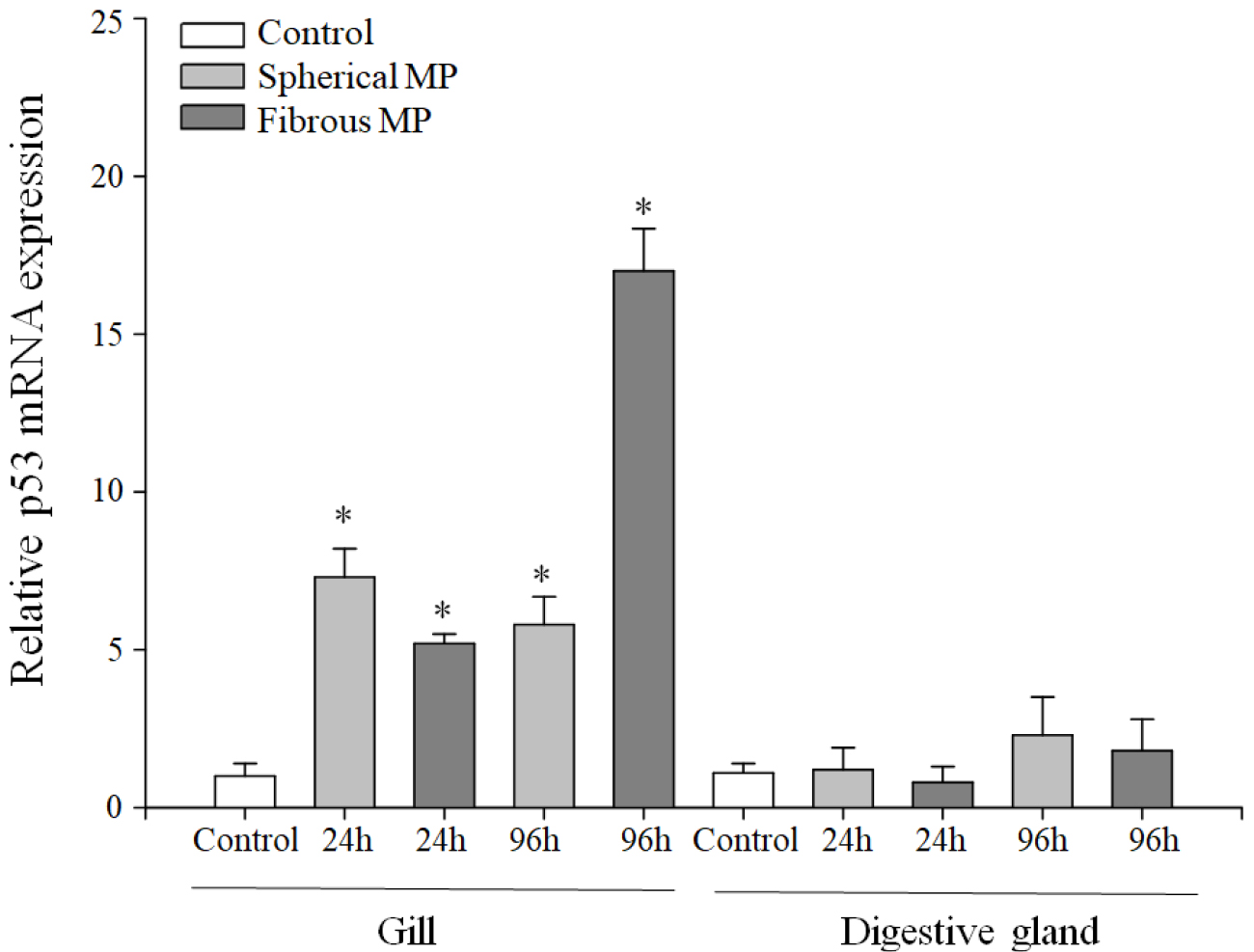
Fig. 7.
Relative expression of the p53 gene in the gill and digestive gland of Mytilus galloprovincialis mussels exposed to spherical and fibrous MPs for 24 and 96 h. The expression of the target gene was normalized to that of β-actin. The data present as mean ± standard deviation (n = 3). The asterisks (*) indicate statistically significant differences (* p < 0.05)
4. 결 론
본 연구는 지중해담치에서 구형과 섬유형 MP 노출에 따른 체내축적과 세포독성의 증가 및 세포사멸 p53 유전자의 발현 변화를 확인하였다. 구형 MP 노출은 24시간에 체내축적이 높게 나타났으며 96시간에는 상대적으로 감소하였다. 하지만 섬유형 MP는 노출시간 의존적으로 체내축적이 증가하였지만, 세포독성 영향은 노출 조직과 시간에 따라 다르게 나타났다. 아가미 조직이 소화선 조직에 비해 MP 노출에 따른 세포독성 증가가 뚜렷하게 관찰되었다. 노출 24시간에 아가미 조직은 상대적으로 고농도의 구형과 섬유형 MP의 노출에만 세포독성이 확인되지만, 96시간에는 노출농도 의존적으로 세포독성 증가가 전체적으로 나타났다. 하지만 소화선 조직에서는 MP 노출에 따른 유의적 세포독성 증가가 관찰되지 않았다. 또한 세포사멸(apoptosis) 관련 유전자인 p53의 발현도 아가미 조직에서는 대조군에 비해 통계적으로 유의한 수준으로 증가하였다. 이는 지중해담치에서 구형 MP 보다 섬유형 MP의 섭취가 세포사멸을 유도하는 높은 세포독성을 일으키는 환경위해성을 유도함을 시사한다. 나아간 연구에서는 다른 형태와 더불어 polymer 종류가 다른 MP 노출에 대한 세포독성 반응도 확인되어야 할 것이다.