1. 서 론
2. 재료 및 방법
해파리 시료 채집 및 DNA 추출
해파리 유전자 증폭 및 DNA 시퀀싱
염기서열 유사도, 유전거리 및 분자계통 분석
3. 결과 및 고찰
커튼원양해파리의 핵 rDNA와 미토콘드리아 COI 염기서열 특성
미토콘드리아 COI을 이용한 Chrysaora 속의 분자계통 추정
한국 커튼원양해파리의 분자지리적 유연관계
4. 요약 및 결론
1. 서 론
최근 전 세계적으로 해파리 대량발생이 빈번하게 일어나고 있으며, 이는 해양 생태계 먹이사슬 불균형의 원인이 되고 있다(Mills 2001). 해파리는 유성생식 및 폴립의 무성생식에 의하여 환경이 양호할 경우 기하급수적으로 증가하는 생물학적 특성을 지니고 있다(Arai 1997). 해파리의 대량발생은 먹이생물인 동물플랑크톤과 치어에 대한 대량 섭식으로 이어지고, 어류의 먹이 및 개체군 감소에 따른 수산자원의 손실과 생태계 불균형을 초래한다(Kawahara et al. 2006). 또한 대량 출현한 해파리 개체의 사망과 부패로 인하여 수계 내에 용존 산소 감소와 암모니아 증가로 인해 해양 환경에 치명적인 변화를 야기한다. 이러한 해파리의 대량발생은 지구온난화, 환경오염의 심화, 해양 인공구조물 구축, 수산자원 고갈 등이 주요 원인으로 제기되어 왔다(Arai 2001; Graham 2001; Parsons and Lalli 2002; Uye and Ueta 2004; Yasuda 2004; Purcell 2005). 따라서 지금까지 세계적으로 유해 해파리를 대상으로 생활사, 생태, 이동경로 및 분포, 수산 자원측면의 연구, 쏘임 사고 응급처치방법 및 독성물질의 규명과 관련된 연구가 다양하게 수행되어 왔다(Behrends and Schneider 1995; Brodeur et al. 1999; Yoshimoto and Yanagihara 2002; Kinoshita et al. 2006; Yoon et al. 2008).
한국에서는 1990년대 후반부터 보름달물해파리가 남해 마산만과 서해안 일대에서 대량으로 출현하기 시작하면서 점차 사회적 문제로 대두되었다(Chung et al. 2012). 현재까지 해파리의 대량발생에 따른 직접적, 간접적 피해가 매년 수 백억에서 수천억 원에 이를 정도로 피해가 급격하게 증가하고 있다(Kang et al. 2010). 이로 인해 국립수산과학원에서는 해파리정보센터의 운영을 통해 해파리 실시간 모니터링, 해양환경과의 관계, 제어연구 등 해파리에 관련된 연구 활동을 활발하게 진행하고 있다. 한국 수역에서는 매년 30여종의 해파리가 출현하는데, 대량발생으로 많은 피해를 입히는 종으로는 보름달물해파리(Aurelia aurita)와 노무라입깃해파리(Nemopilema nomurai)가 대표적으로 보고되어왔다(Kim et al. 2014). 최근에는 다양한 해파리(예, 유령해파리, 작은상자해파리, 커튼원양해파리)의 출현이 빈번해지고 있다(Lee et al. 2016; Chae et al. 2018).
커튼원양해파리는 해파리강 기구해파리목 원양해파리과에 속하며, 주로 대서양이나 인도태평양의 아열대 바다에서 나타난다. 최근에는 지구온난화로 인해 일본 근방의 태평양 북부에서도 출현한 보고가 있다(Uchida 1970; Toyokawa 2011). 한국의 커튼원양해파리(Dactylometra quinquecirrha Agassiz, 1862)에 대한 기록은 2000년 거제도에서 최초로 보고되었다(Park 2002). 하지만 D. quinquecirrha는 멕시코 만에만 제한적으로 서식하는 것으로 보고되었으며(Morandini and Marques 2010), 한국과 다른 지역에서 보고된 D. quinquecirrha에 대해서는 종 동정의 의문이 제기되어 왔다(Lee et al. 2013). 최근 한국에서 알려진 커튼원양해파리(D. quinquecirrha)의 형태학적 및 분자생물학적 자료를 이용하여, 학명을 Chrysaora pacifica (Goette, 1886)로 새롭게 기재하였다(Lee et al. 2016). 한국의 커튼원양해파리는 주로 여름철 남해안에 분포하는 것으로 알려져 왔으나(Park 2002; Lee et al. 2016), 최근 해파리 모니터링에 의하면 동해안에도 유사한 종이 목격되고 있다. 하지만 이들에 대한 연구는 거의 실시되지 않았다.
본 연구에서는 한국의 동해 해역에 출현한 커튼원양해파리의 유전자 염기서열을 분석하여 남해안에 출현하는 커튼원양해파리와의 지리적 유연관계를 분자계통학적으로 규명하였다.
2. 재료 및 방법
해파리 시료 채집 및 DNA 추출
2013 ~ 2015년 해파리 연간 조사를 통해 동해(고성, 양양, 속초)와 남해(통영, 거제) 해역에서 총 15개체의 커튼원양해파리를 채집하였다(Table 1). 핸드 네트와 플라스틱 용기를 사용하여 해파리 성체를 채집하고, 우산 직경을 측정하였다. 형태 관찰을 위해 니콘 카메라(D810, Tokyo, Japan)로 사진을 촬영하였으며, 세부 관찰을 위해 5% 포르말린으로 조직을 고정하였다. 유전자 분석을 위한 시료는 촉수와 근육조직을 100% 에탄올(Merk, Darmstadt, Germany)로 고정하였다.
알코올에 고정된 해파리 시료로부터 genomic DNA (gDNA)를 추출하였다. 증류수로 시료를 세척하고 60°C 오븐에서 완전히 건조하였으며, 이후 cetyl trimethylammonium bromide (CTAB) 방법으로 DNA를 추출하였다(Richards et al. 2003).
Table 1.
Origins of Chrysaora pacifica specimens examined and GenBank accession numbers for nuclear ITS rDNA, including 5.8S, and mitochondrial COI gene sequences
해파리 유전자 증폭 및 DNA 시퀀싱
해파리의 핵 5.8S rRNA와 internal transcribed spacer (ITS) rDNA 영역과 미토콘드리아 cytochrome c oxidase subunit 1 (COI) 유전자를 효소중합연쇄반응(PCR)으로 증폭하였다. 핵 ITS 증폭을 위해 진핵생물 범용 프라이머 세트(18F01, 5′-TAT CTG GTT GAT CCT GCC AGT AG-3′, 28R691, 5′-CTT GGT CCG TGT TTC AAG AC-3′)를 사용하였고, 미토콘드리아 COI은 mitoCOI 범용 프라이머 (Fco04, 5′-CAA CAA ACC ATA AAG ATA TAG GAA C-3′, Rco800, 5′-TAT TGC TAT CAT AGC ATA AAC CAT-3′)를 이용하였다. PCR은 추출한 gDNA 2 µL, ITS와 COI 프라이머를 각각 넣은 PCR 반응액(23 µL)을 혼합하여 실시하였다. PCR 반응액은 1 × PCR buffer, 0.2 mM dNTPs, 0.5 mM forward-reverse 프라이머, 1 unit Ex Taq polymerase (Takara Bio, Shiga, Japan)를 사용하였다. PCR 반응은 MyCycler™ (Biorad, Hercules, CA)를 이용하여 초기 94°C 3분간 DNA를 변성 시키고, 이후 94°C 20초, 55°C 30초, 68°C 5분을 35회 반복하여 대상 유전자 영역을 증폭하였다. PCR 증폭 반응이 종료되면 추가로 72°C 5분간 유지하여 반응을 종결하였다. 증폭된 PCR 산물은 1% 아가로스 겔에서 전기영동한 후 관찰하였다.
DNA sequencing은 PCR 산물을 PCR purification kit (Bionics Co., Seoul, Korea)로 정제하여, PCR 프라이머와 ABI PRISM® BigDyeTM Terminator Cycle Sequencing Ready Reaction kit (PE Biosystems, CA)를 이용하여 실시하였다. DNA sequencing 단편은 자동 DNA 분석기(Model 3700, Applied Biosystems, CA)로 분석하였다. 각각의 시료로부터 얻은 염기서열 단편을 Sequencher 4.1.4 (Gene Codes, MI)을 이용하여 조합된 단일 염기서열로 만들고, 염기서열을 GenBank에 등록하였다(Table 1).
염기서열 유사도, 유전거리 및 분자계통 분석
한국의 커튼원양해파리 Chrysaora pacifica ITS+5.8S rDNA와 COI 유전자의 염기서열 유사도(DNA similarity)와 유전거리(genetic distance)를 분석하였다. 본 연구에서 규명한 염기서열로 데이터 조합을 만들고, BioEdit 소프트웨어(http://www.mbio.ncsu.edu/BioEdit/bioedit.html)를 이용하여 염기서열 재배열(alignment)한 후, 같은 길이가 되도록 양 끝을 제거하였다. 이후, BioEdit를 이용하여 유사도를 계산하고, MEGA 6.0 (http://www.megasoftware.net)에서 Kimura 2-parameter 모델을 이용하여 유전거리를 계산하였다. 통계분석은 SPSS 10.0.7 (SPSS, Chicago, IL)을 이용하였다.
커튼원양해파리를 포함하는 Pelagiidae과(family) 해파리의 미토콘드리아 COI 유전자 염기서열을 이용하여(Table 1), Maximum Likelihood (ML) 계통분석을 실시하였다. 분석은 COI 염기서열을 MAFFT 소프트웨어(Katoh and Standley 2013)로 재배열하고, 이 후 양 끝을 동일한 크기로 자른 후 데이터 세트를 준비하였다(COI, 900 sites에서 584 sites 선택). ML 계통도는 GTR nucleotide substitution model을 이용하여 RAxML 8.0로 추정하였다(Stamatakis 2014). ML tree는 TreeView 1.6.6 (Page 1996)로 시각화 하였다.
한국의 커튼원양해파리 COI 유전자를 이용하여 지리적 계통유연관계를 파악하였다. 계통지리분석은 위에 사용한 방법으로 분석할 염기서열을 재배열하고, neighbor-joining (NJ) 알고리즘을 이용하여 추정하였다.
3. 결과 및 고찰
커튼원양해파리의 핵 rDNA와 미토콘드리아 COI 염기서열 특성
본 연구에서 채집한 동해 지역 고성, 양양, 속초 해역의 커튼원양해파리는 약 15 cm의 우산 직경(umbrella diameter), 둥근 모양의 가장자리 lappet, 32개의 갈색 방사 스트립(radial stripe)과 40개의 촉수를 갖고 있다(Fig. 1). 이와 같은 특징은 한국 남해에서 보고된 커튼원양해파리와 일치하므로(Chae et al. 2018), 동해에서 조사한 해파리가 같은 종이라는 것을 형태적으로 뒷받침한다.
본 연구에서는 남해(통영, 거제)와 동해에서 채집한 커튼원양해파리 15개체의 핵 5.8S rRNA를 포함한 ITS rDNA 영역과 미토콘드리아 COI 유전자의 염기서열을 규명하여(Table 1), 이들 지역의 유전적 특성을 비교하였다. 동해 커튼원양해파리의 전체 ITS rDNA 염기서열은 586 bp (5.8S rDNA 158 bp, 50% GC 포함)로 조사되었다. Blast 검색결과 GenBank에 등록된 Chrysaora pacifica (GenBank 번호 KY212123; Chae et al. 2018)와 100% 일치하는 것으로 파악되었다. 또한, 미토콘드리아 COI 부분 염기서열 716 bp를 분석하였으며, GenBank 데이터베이스에서 Blast 검색으로 일본 마이즈루시에서 채집된 C. pacifica (GenBank 번호 LC191575)와 99.9% 일치하는 것으로 파악되었다. 본 분석 결과는 동해에 출현하는 커튼원양해파리가 분자유전학적으로 C. pacifica라는 것을 제시한다. 또한, 본 연구의 15개체 ITS 염기서열 분석은 양양 1개체(YYNA02)의 99.3%를 제외하고, 14개체간에 100% 유사도를 보였으며, 15개체 미토콘드리아 COI 부분 염기서열 비교에서는 98.7% 이상의 유사도를 갖는 것으로 파악되었다(Table 2). 따라서, 커튼원양해파리는 핵 ITS rDNA 보다 미토콘드리아 COI 염기서열의 변이가 높은 것으로 판단된다.
Table 2.
Similarity scores of mitochondrial COI (above diagonal) and nuclear ITS+5.8S rDNA (below diagonal) calculated by the aligned sequence data of the partial COI gene and complete ITS, including the 5.8S rDNA gene, from Korean Chrysaora pacifica
미토콘드리아 COI을 이용한 Chrysaora 속의 분자계통 추정
지금까지 커튼원양해파리에 대한 분자계통학적 연구는 핵 18S rDNA를 이용하여 강(class), 목(order), 또는 과(family) 수준에서 대부분 실시되어 왔다(Bayha et al. 2010; Rizman-Idid et al. 2016). 최근에 Chryaora 속의 핵 28S rDNA와 미토콘드리아 COI, 16S rRNA 유전자를 이용하여 미국에 출현하는 C. quinquecirrha와 C. chesapeakei의 지리적 분리특성이 규명되었다(Bayha et al. 2017). 또한, 본 연구팀은 한국 남해 C. pacifica의 핵 rDNA 전장 염기서열을 규명하였으며, 이를 이용하여 커튼원양해파리의 계통유연관계를 규명하였다(Lee et al. 2016; Chae et al. 2018). 본 연구에서는 해파리 미토콘드리아 COI을 이용하여 Pelagiidae 과의 계통유연관계를 파악하였다(Fig. 2). Chrysaora 속은 단계통군(monophyletic)을 형성하였으며, 다른 분류군(예, Mawia, Pelagia, Sanderia 속)과 뚜렷하게 분리되어 서로 구별되지 않았던 18S rDNA 및 28S rDNA 계통분석에서와 다른 결과를 보였다. 특히 해파리 COI은 본 연구에 사용한 Chrysaora 속 18종을 뚜렷하게 분리하였으며, 18S와 28S rDNA 분자계통 연구에서(Chae et al. 2018) 구별하지 못하는 C. fuscecens, C. melanaster, C. colorata의 관계를 잘 설명하였다. 한국 시료와 GenBank에서 얻은 커튼원양해파리 C. pacifica는 모두 단일 clade를 묶였으며, 이 종은 C. chinensis와 근연관계를 형성하였다. 이러한 결과는 Chrysaora 종을 분류하기 위해 핵 18S와 28S rDNA 유전자 보다 미토콘드리아 COI 유전자 염기서열이 더 적합하다는 것을 제시한다.
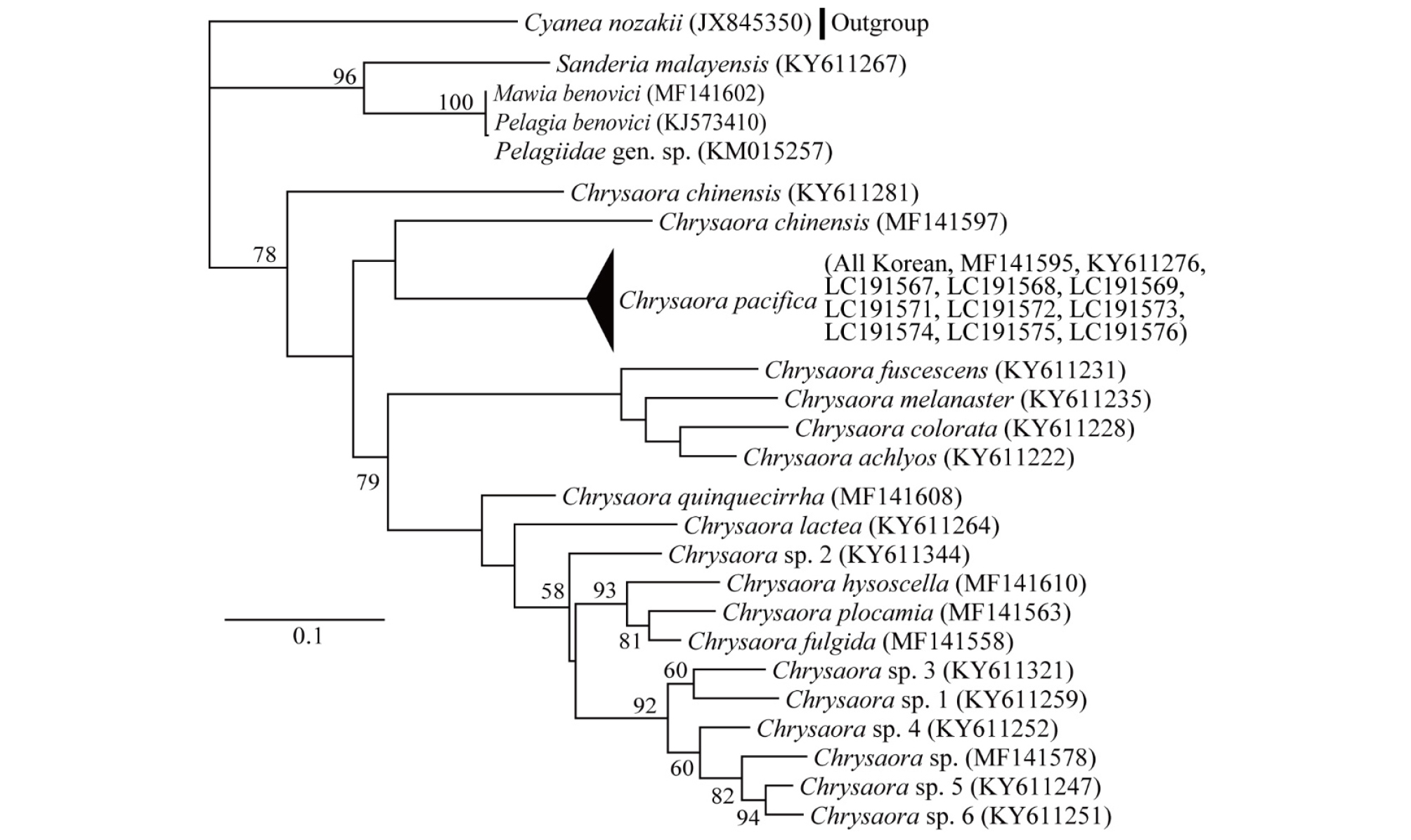
Fig. 2.
Phylogenetic relationships of the jellyfishes within the family Pelagiidae inferred from mitochondrial COI sequences and maximum-likelihood (ML) algorithms. The ML analysis was used as the nucleotide substitution model of GTR+G. DNA sequences used here are openly available in GenBank with the given accession numbers as parenthesis. Cyanea nozaki (Cyaneidae) was included as the outgroup. Bootstrap proportions (BP) (> 50%) in ML were incorporated into the ML tree to support the strength of each branch. Branch lengths are proportional to the scale given
한국 커튼원양해파리의 분자지리적 유연관계
한국 남해와 동해에 출현한 C. pacifica의 지리적 근연관계를 미토콘드리아 COI 유전자와 NJ 알고리즘으로 분석하였다(Fig. 3). 본 연구에서 동해 고성에서 채집한 1 개체(GS03)를 제외하고, 14개 개체들이 지역별로 뚜렷하게 분리되었다. 본 연구에서 동해 해역에 출현한 개체들과 남해 해역에 출현한 개체들이 모두 동일한 종으로서 판명되었지만(Fig. 2), 이들 두 지역의 커튼원양해파리가 개체군 수준에서 유전적으로 다르다는 것을 제시한다. 한국에 출현하는 커튼원양 해파리의 발생 빈도와 해류의 이동방향으로 추정할 때, 동해 C. pacifica개체군은 해류를 통해 남해 해역으로부터 유입되어 출현하였을 가능성이 있다. 현재는 한국 남해와 동해의 커튼원양해파리의 발생빈도가 낮아 해파리 개체군 분석을 위한 충분한 시료를 확보하지 못하였으나, 향후 시료 수를 충분히 확보하여 이들 지역의 개체군 집단유전 분석이 필요하다.
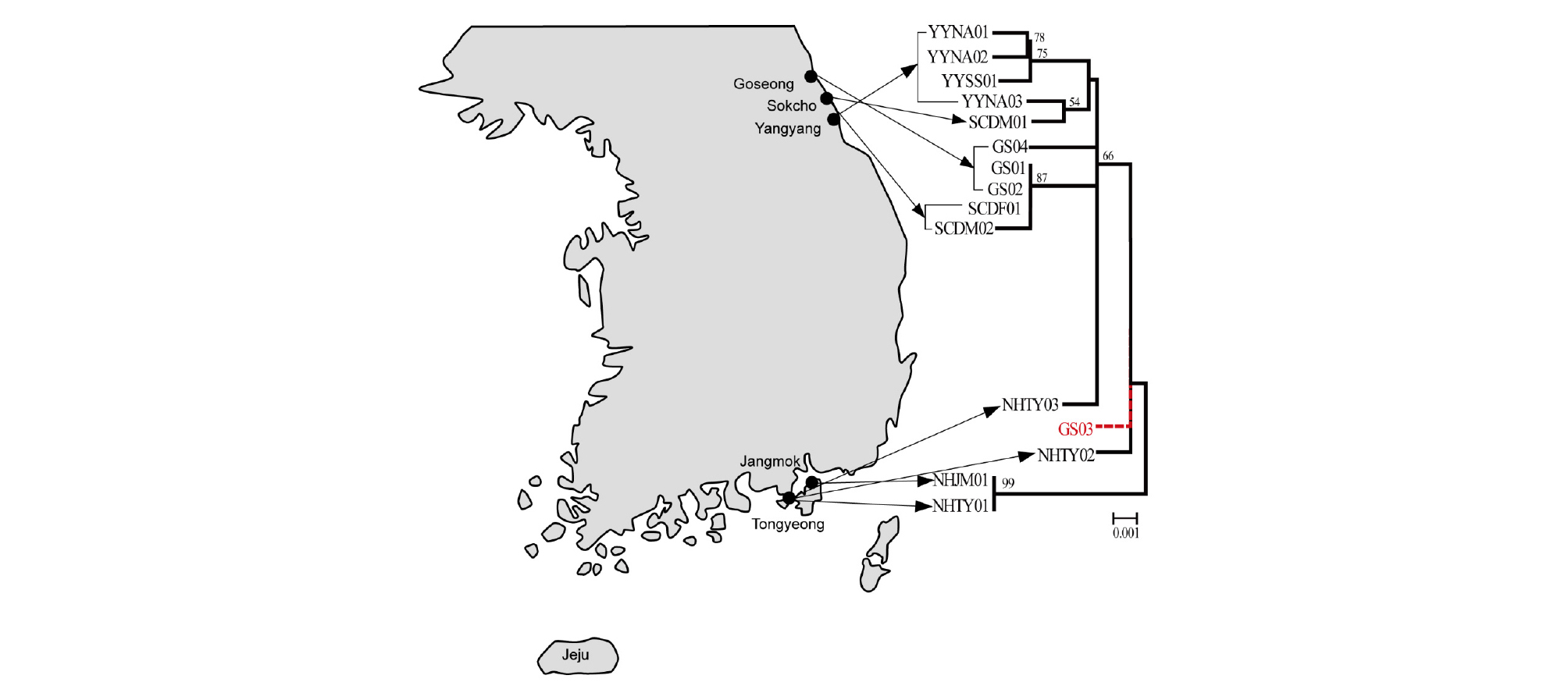
Fig. 3.
A map and phylogeographic relationships of Korean Chrysaora pacifica showing their geographical distributions. The tree was inferred from neighbor-joining (NJ) algorithm using mitochondrial COI sequences of C. pacifica. The numbers above the nodes are bootstrap values (percentage). A dotted line indicates that it is not grouped to the same geographic clusters
커튼원양해파리 집단유전 연구를 위한 미토콘드리아 COI 유전자와 핵 ITS rDNA 변이를 p-distance를 이용하여 파악하였다(Fig. 4). COI 유전자 변이는 ITS rDNA 유전자 변이에 비해 약 7 배 정도 높은 것으로 파악되었으며, 통계적으로 유의한 차이를 보였다(Student t-test, P < 0.05, N = 15). 이와 같은 변이는 COI 분자계통분석의 높은 해상도를 잘 설명하여 준다. 이것은 미토콘드리아 COI 유전자가 핵 ITS rDNA에 비해 변이가 높으며, C. pacifica를 구분하기 적합한 분자 마커라는 것을 제시한다.
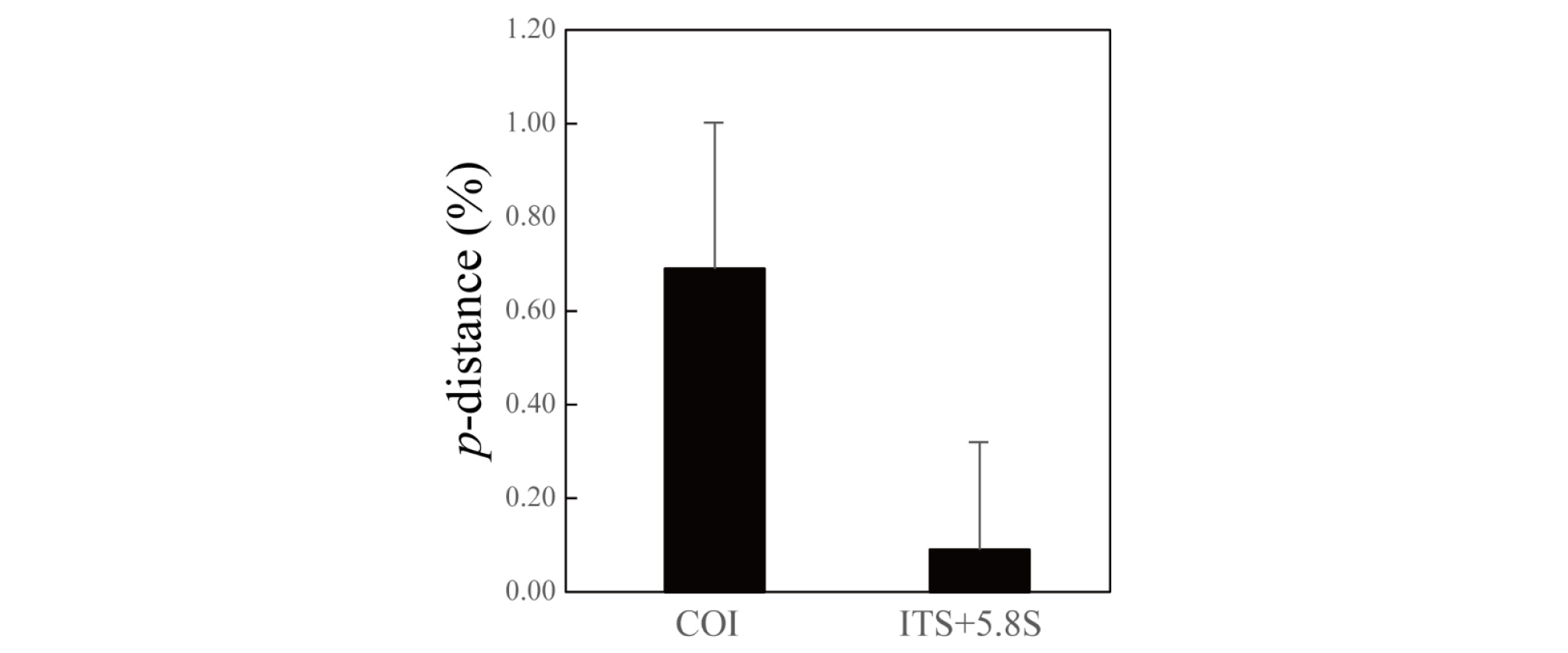
Fig. 4.
Nucleotide divergences of mitochondrial COI and nuclear ITS+5.8S rDNA of the Korean Chrysaora pacifica. Genetic distances between each paired sequence were calculated by a Kimura 2-parameter model. Statistical analysis showed that the COI divergences were significantly different against those of ITS rDNA (Student t-test, P < 0.05, N = 15)
4. 요약 및 결론
한국의 남해에 출현하는 커튼원양해파리의 분포와 유전형이 파악되었으나, 동해에서는 거의 규명되지 않았다. 본 연구는 형태적으로 동해 연안(고성, 양양, 속초)에 출현한 커튼원양해파리를 분류하였으며, 이들의 유전형을 남해(통영, 거제) 시료와 비교하였다. 미토콘드리아 COI 유전자를 이용한 분자계통분석에서, Chrysaora 속은 다른 분류군과 명확이 분리되어 단계통군을 형성하였으며, 각각의 종들이 뚜렷하게 분리되었다. 동해와 남해의 커튼원양해파리가 COI 유전자 계통분석에서 지역별로 분리되었으며, 다른 개체군 집단의 가능성을 제시한다. 한국 커튼원양해파리 COI 유전자는 핵 ITS rDNA 보다 7배 정도 유전적 변이가 있으며, 향후 커튼원양해파리 집단유전 분석을 위한 유용한 마커로 사료된다.





