1. 서 론
꼬시래기류(Gracilariacean spp.)는 한천 산업의 원료로서 경제적 가치가 높으며(Zemke-White and Ohno 1999; Polifrone et al. 2006), 높은 생장률과 영양번식의 적합성 때문에 활용할수 있는 장점이 많은 홍조류이다(Kain and Destombe 1995; Michetti et al. 2013). 최근, 산업적 활용의 증가 및 다양한 양식방법의 개발을 위해서 자연개체군이 과도하게 채집되었다(Mantri et al. 2009). 꼬시래기류의 영양번식기술 양식은 엽체 연령과 집중된 수확으로 인하여 2 ~ 3년 후에는 생산성 감소가 일어났다(Buschmann et al. 1995). 인공적인 영양번식(vegetative propagation)은 노동-집약적이고 양식 종묘 확보를 위한 대량 채집으로 이어져 자연개체군의 생물량 감소를 유발하므로 연안생태계 건강에 부정적이다(Jayasankar and Varghese 2002). 영양번식 양식의 문제점을 해결하기위하여, 대량 양식을 해조류 포자로 시작하는 포자양식방법이 대규모 상업양식 방법으로 제안되었다(Alveal et al. 1997). 사분포자와 과포자 모두를 사용한 비교 실험 결과, 과포자는 배수체(diploid)이며 활성이 높고(Mantri et al. 2009), 암배우체의 엽체 위에서 성숙 상태를 육안으로 쉽게 확인 가능한 낭과로부터 확보할 수 있어서 포자양식방법에 주로 활용된다(Glenn et al. 1996).
한국의 꼬시래기[Agarophyton vermiculophyllum (Ohmi) Gurgel, J.N. Norris & Fredericq]는 암반, 자갈, 플라스틱 조각 등 다양한 기질에 부착하며 조수웅덩이와 하구까지 다양한 염분 농도에서 잘 서식한다(Choi et al. 2006). 꼬시래기 양식 연구는 생장과 성숙시기를 파악하기 위한 연구(Kim et al. 1998), 포자양식방법 중 종묘생산을 위한 사분포자와 과포자 방출 유도 방법 연구(Kim et al. 2001), 그리고 엽체 영양양식을 위한 해면 양식 연구(Choi et al. 2006) 등이 수행되었다. 특히, Kim et al. (2001)이 사용한 사분포자와 과포자방출 유도방법은 건조충격, 암조건 후 광충격, 담수충격의 3가지 방법으로, 건조기간, 암기간, 담수충격 기간별 방출량을 계수하였다. 꼬시래기류의 포자 채묘양식방법의 시작은 다량의 포자를 확보하기 위한 포자방출유도 방법의 개발에 있으며, 포자방출 유도방법은 꼬시래기의 속(genus) 내에서도 종에 따른 차이를 나타냈다(Guzmán-Urióstegui and Robledo 1999; Michetti et al. 2013).
본 연구의 목적은 꼬시래기의 과포자를 이용한 채묘양식기술 개발을 위하여 다량의 포자 확보를 위한 최적 포자 방출 유도방법을 파악하고자 하였다.
2. 재료 및 방법
과포자 방출 유도
꼬시래기 과포자체는 충남 보령군 무창포 해안에서 2017년 9월에 채집하여 해수와 함께 실험실로 운반하였다. 해부현미경을 이용하여 성숙한 과포자체에서 착생 동・식물을 제거하고 멸균해수로 수 회 세척한 후, 10개의 낭과를 가진 길이가 2 ~ 3.5 cm인 15개의 엽체 절편을 준비하였다.
꼬시래기 낭과로부터 다량의 과포자를 일시에 확보하기 위하여, 선행연구에서 최대 방출량을 보인 자연방출(Michetti et al. 2013)을 포함하는 5 종류의 포자방출 유도방법(자연방출, 건조, 저온, 저온・건조, 삼투충격)을 적용하였다. 방출된 과포자 수는 2일 간격으로 계수하였고 개별 낭과의 일별 과포자 수를 계산하였다. 자연방출 유도방법에서 전처리는 실온에서 Plant culture dish (Ø 10 cm)에 엽체 절편 3개를 멸균해수(100 mL)와 함께 보관하였다. 건조충격(desiccation shock) 포자방출 유도방법 전처리는 수분을 제거한 엽체 절편 3개를 Plant culture dish에 넣고 알루미늄 호일로 광을 차단한 암조건에서 2 h 동안 실온 보관하였다. 저온충격(low-temperature shock) 전처리는 5℃의 멸균해수(100 mL)와 엽체 절편 3개를 Plant culture dish에 넣고 호일로 감싼 후 2 h 동안 5℃로 세팅된 배양기(Bionex, Korea)에서 보관하였다. 건조+저온충격(desiccation and low-temperature shock) 포자방출 방법에서 전처리는 수분을 제거한 엽체 절편 3개를 Plant culture dish에 넣고 광을 차단한 후 5℃에서 2 h 동안 보관하였다. 삼투충격(osmotic shock) 전처리는 염분농도가 60 psu인 실온의 인공해수에서 30분간 보관하였다.
전처리한 15개의 엽체 절편(실험구별 3개)은 15 mL의 PES 배양액(Provasoli 1968)을 넣은 Petri dish (Ø 5 cm)에 한 개씩 분배한 후, 25℃, 60 µmol photons m-2 s-1와 16:8 h L:D (Light : Dark)로 세팅된 배양기에서 6일 동안 배양하였다. 배양기의 광원은 형광등이었고 광도는 디지털 조도계(Takemura, DX–200, Japan)로 확인하였다. 각 엽체 절편은 2일(48 h) 마다 새로운 배양액으로 옮기고 과포자 현탁액(15 mL)을 균질하게 혼합한 후 1 mL씩 채취하여 Sedgewick-rafter chamber에 넣어 광학현미경(Olympus, BX53F, Japan) 하에서 전량 계수하였다. 방출된 포자는 반복구별로 1 ml씩 3회(총 3 mL)를 계수하여 평균값을 사용하였다.
온도가 꼬시래기 과포자 방출에 미치는 영향을 파악하기 위하여, 저온・건조 충격으로 전처리한 엽체 절편(낭과 10개씩 가짐)을 9개 준비하였고 PES 배지가 담긴 9개의 Petri dish에 각 절편 한 개씩을 분배하였다. 각기 다른 온도(20, 25, 30℃)에서 5일 동안 배양하면서 방출된 포자를 24 h 간격으로 계수하였다(3회 반복 검증). 모든 배양기의 광도와 광주기는 60 µmol photons m-2 s-1과 12:12 h L:D로 동일하였다.
일장과 광도의 조합이 꼬시래기 과포자 방출에 미치는 영향을 파악하기 위하여, 건조×저온 충격으로 전처리된 꼬시래기 절편을 서로 다른 3개의 일장(8, 12, 16 h)과 2가지 다른 광도(30, 60 µmol photons m-2 s-1)에서 5일간 배양하였다. 모든 배양기의 온도는 25℃로 동일하였고, 실험구별로 3개의 반복구를 두었다.
통계분석
꼬시래기 과포자 방출에 환경이 미치는 영향을 파악하기 위하여 통계분석을 실시하였다. 데이터의 동질성은 Cochran’s test를 이용한 등분산검정(homogeneity of variances)법을 적용하였으며, 과포자 방출에 대한 유도방법과 온도의 영향과 같은 단일 환경요인 실험은 one–way ANOVA test로, 광도×일장이 조합된 실험에서는 two–way ANOVA test로 유의차를 검정하였다. 평균에 대한 유의차가 발견되면 Tukey’s HSD test 방법으로 사후 검정하였으며(Sokal and Rohlf 1995), 데이터 분석을 위해 사용된 통계 프로그램은 STATISTICA version 5.0 이었다.
3. 결 과
포자방출 유도방법별 포자량
꼬시래기 과포자 방출은 다양한 방출유도방법(자연방출, 건조, 저온, 건조+저온, 삼투 충격)에서 모두 일어났으며, 배양 2, 4일 경과 시 6일 경과에 비해 과포자가 대량으로 방출되었다. 과포자 방출 실험에서 6일 동안 한개의 낭과에서 방출된 총 포자수가 676 ~ 4,090 spores/cystocarp로서 건조+저온충격 방법에서 최대였으며, 삼투충격 조건에서 최소였다. 꼬시래기 낭과별 포자 방출량은 5개 조건에서 일평균 306개 포자였으며, 건조+저온충격 방법이 삼투 충격 방법에 비해 약 7배 많은 포자방출량을 보였다. 건조 혹은 저온충격 중에서 하나의 방법을 사용한 것에 비해서도 통계적인 유의차를 보일 정도로 방출량이 많았다(P < 0.001, Fig. 1). 과포자방출을 유도하기 위하여 실험한 60 psu의 고염해수에 의한 삼투충격을 주었을 때 방출된 과포자의 양도 적었으며, 이때 방출된 포자는 활성이 없었다.
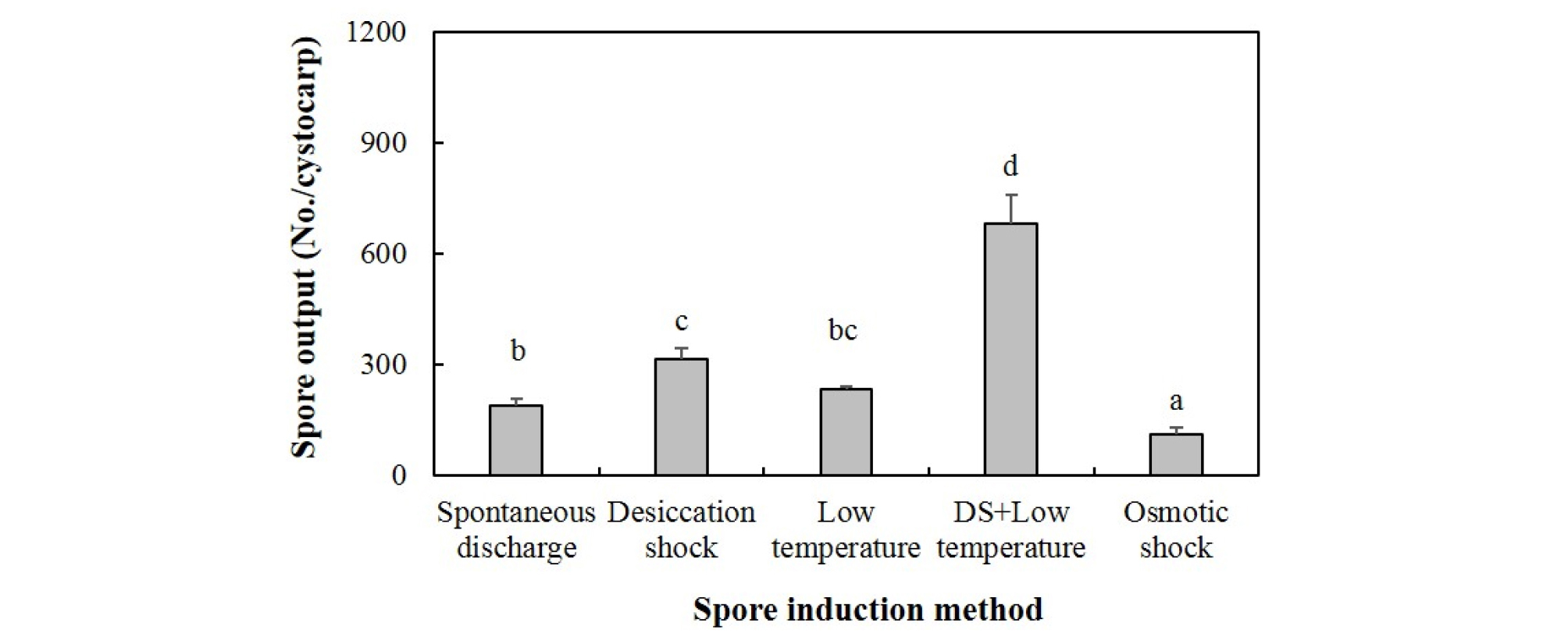
Fig. 1.
Average number of carpospores daily released per cystocarp in A. vermiculophyllum under five different spore induction methods. Experiments ran for 6 days at 25°C and 60 µmol photons m-2 s-1 and 12:12h L:D. Different letters represent significant differences. Vertical bars indicate mean ± SE (n = 3 replicates). DS, Desiccation shock
포자방출과 온도, 광도・일장
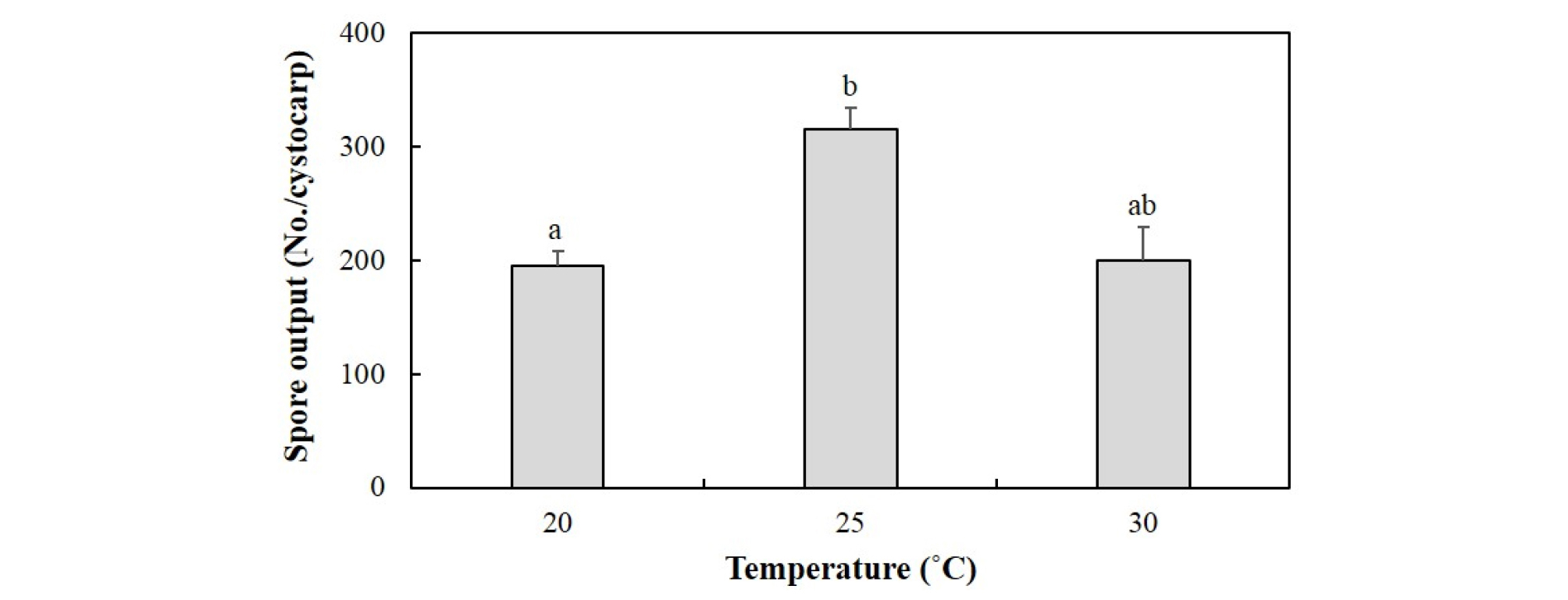
건조+저온충격으로 전처리한 꼬시래기 낭과는 20 ~ 30℃의 모든 실험온도에서 과포자를 방출하였으며, 한 개의 낭과에서 5일 동안 방출된 과포자는 974 ~ 1,576 spores/cystocarp였다. 실험 온도구(20, 25, 30℃)에서 낭과별 일평균 과포자 방출량은 194 ~ 315개로 20℃와 30℃ 조건에 비하여 25℃에서 다량의 포자가 방출되었으며, 포자량에서 유의한 차이를 보였으나(P < 0.01), 20℃와 30℃에서 방출된 포자량은 유의한 차이가 없었다(P > 0.05, Fig. 2).
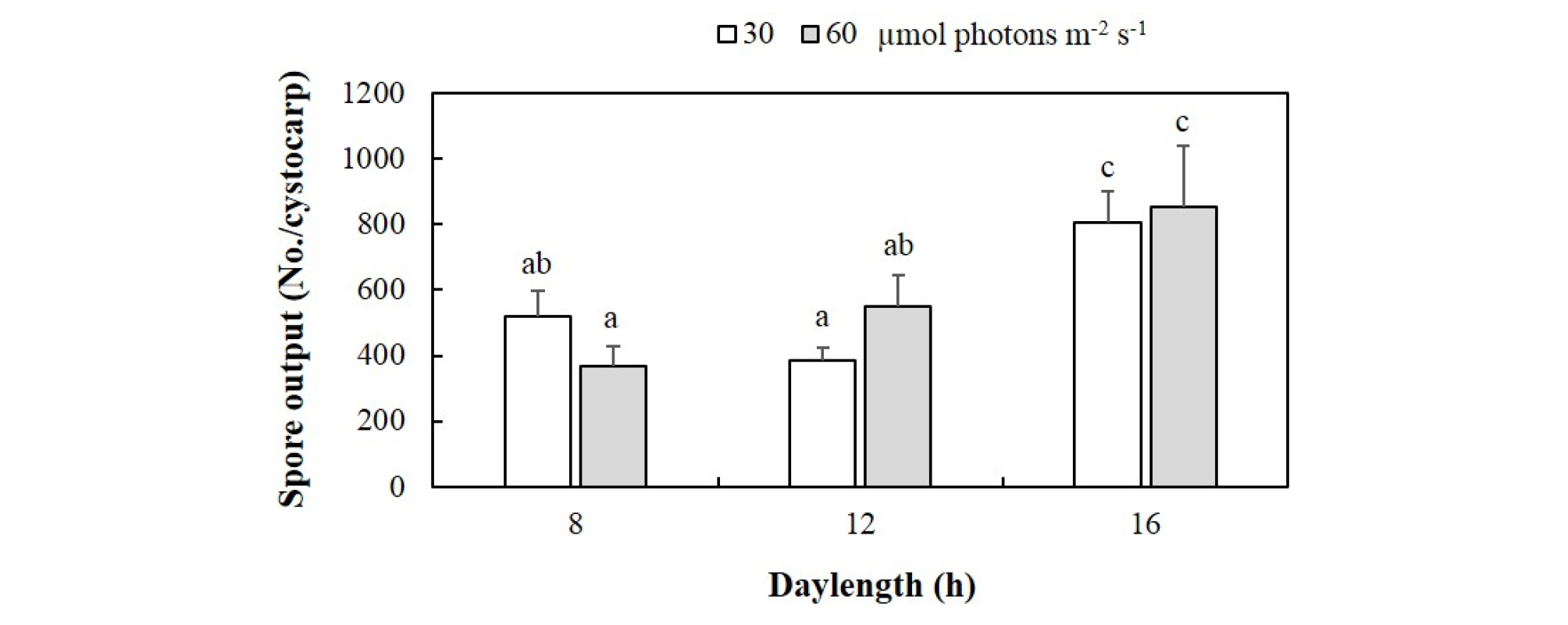
또한, 꼬시래기 낭과에서 진행된 과포자 방출은 다른 광도(30, 60 µmol photons m-2 s-1)와 일장(8, 12, 16 h)이 조합된 환경조건에서도 일어났다(Fig. 3). 낮은 광도(30 µmol photons m-2 s-1)의 경우, 한 개의 낭과에서 5일 동안 방출된 과포자 수는 일장에 따라 1,946 ~ 4,037 spores/cystocarp로서 장일조건(16 h)에서 최대였다. 장일조건에서는 8 h와 12 h의 일장 조건에 비해서 다량의 과포자를 확보할 수 있었으며(P < 0.001), 8 h와 12 h 일장조건에서는 유의한 차이를 보이지 않았다(P > 0.05). 한편, 60 µmol photons m-2 s-1에서 방출된 포자는 1,847 ~ 4,277 spores/cystocarp로서 장일조건(16 h)에서 최대였으나(P < 0.001), 2개의 광도조건에서는 유의한 차이가 없는 것으로 확인되었다(P = 0.588, Fig. 3). 포자방출에 영향을 미치는 광도와 일장의 상호작용이 확인됨으로써 일장에 따라 광도의 영향이 다르게 영향을 주는 것으로 확인되었다(Table 1, Fig. 3).
4. 고 찰
꼬시래기 과포자 확보를 위한 5가지 전처리 방법 중에서 건조+저온 충격 방법이 최적인 것으로 확인되었으며, 25℃의 장일 조건(16 h)에서 배양 3 ~ 4일 후에 방출량은 최대였으나 광도별 차이는 없었다. 선행 연구에서 많은 연구자가 실내배양 혹은 야외양식을 위한 채묘를 위하여 다양한 방법으로 꼬시래기류(Gracilaria spp.)의 과포자와 사분포자 방출을 유도하였으며(Table 2), 그 중에서 3가지 방법(자연방출, 삼투충격, 부분건조)이 주로 사용되었다. Gracilaria gracilis의 과포자는 자연방출에서 최대였으며, G. cornea의 과포자 방출량은 3가지 방법에서 차이가 없었다(Table 2). 꼬시래기류의 포자방출은 종별, 생활사 단계(사분포자체, 과포자체)와 환경조건(온도, 광도, 광주기 등)에 따라 다르게 나타났다. 예를 들면, Mantri et al. (2009)는 Gracilaria dura의 과포자 방출은 24℃, 12: 12h L:D와 15 µmol photons m-2 s-1에서 최대였고, G. pacifica의 과포자 방출은 온도와 광도의 영향을 받았다고 하였으며(Garza-Sanchez et al. 2000), G. edulis의 과포자 방출은 고온에서 감소한다고 하였다(Rama Rao and Thomas 1974). 국내에서 Kim et al. (2001)은 꼬시래기(A. vermiculophyllum) 낭과에서 과포자 방출을 유도하기 위한 3가지 방법(건조, 광, 담수 충격)을 시도하였으며, 광충격에서 과포자가 최대로 방출되었음을 확인하였으나, 낭과별 방출된 포자수를 정량화하지 않아서 본 연구 결과와 비교하기는 어려웠다. 하지만, 본 연구에서 사용한 건조+저온 충격 방법은 선행연구에서 과포자의 최대 방출조건으로 알려진 자연방출에 비해 낭과별로 3.6배 이상의 과포자 방출을 유도할 수 있어 꼬시래기의 과포자를 확보할 수 있는 효율적인 방법으로 판단되었다.
온도와 광주기도 꼬시래기의 과포자 방출에 영향을 미치는 중요한 환경요인이었다(Table 2). 꼬시래기 속에 포함되는 많은 종의 과포자 방출을 위한 적온은 20℃ 이상이 5종(Gracilaria corneus, G. foliifera var. angustissima, G. pacifica, G. cornea, G. dura)이었으며, G. gracilis는 13℃로서 다른 종들과 구분되었다(Table 2). 본 연구에 사용된 꼬시래기의 과포자체에서도 포자방출을 위한 최적 수온은 25℃로서 여름철 서해안 수온과 유사하였다. 광주기와 과포자방출의 상관성 연구는 4종(G. gracilis, G. cornea, G. dura, G. arcuate var. arcuate)에 대하여 수행되었으며, Gracilaria cornea와 G. arcuate var. arcuate에서는 8:16h LD에서, 그리고 G. gracilis와 G. dura에서는 12:12h LD에서 최대 방출량을 보였다. 본 연구에서 꼬시래기(A. vermiculophyllum)는 16:8h LD의 광주기에서 최대 방출량을 보임으로써 다른 종에 비해서 장일주기에서 과포자 방출이 잘 일어나는 것을 확인할 수 있었다.
Table 2.
Sporulation experimental conditions of Gracilaria species
| Species | Life stage |
Pretreatment condition | Culture condition | References |
| Gracilaria cornea | Carposporophyte | Spontaneous |
Temp.: 25, 28, 31℃ Irradiance: 10, 25, 50, 75, 100 µmol m-2 s-1 | Orduña-Rojas and Robledo 1999 |
| G. gracilis | Carposporophyte | Spontaneous Osmotic shock Desiccation (1h dark) |
Temp.: 13, 18℃ Irradiance: 10, 30, 60 µmol m-2 s-1 Photoperiod: 8:16, 12:12 h L:D | Michetti et al. 2013 |
| G. foliifera var. angustissima | Carposporophyte | Spontaneous |
Temp.: 16, 18, 20, 22, 24, 26, 28℃ Irradiance: 0, 8, 37, 77 µmol m-2 s-1 | Friedlander and Dawes 1984 |
| G. pacifica |
Tetrasporophyte Carposporophyte |
Spontaneous Spontaneous |
Temp.: 15, 21, 24℃ Irradiance: 0, 60, 140 µmol m-2 s-1 Temp.: 15, 21, 24℃ Irradiance: 0, 60, 140 µmol m-2 s-1 | Garza-Sanchez et al. 2000 |
| G. cornea | Carposporophyte |
Spontaneous Osmotic shock Desiccation |
Temp.: 23, 26, 29℃ Irradiance: 0, 20, 40 µmol m-2 s-1 Photoperiod: 8:16, 12:12, 16:8 h L:D Temp.: 23, 26, 29℃ Irradiance: 0, 20, 40 µmol m-2 s-1 Photoperiod: 8:16, 12:12, 16:8 h L:D Temperature: 23, 26, 29℃ Irradiance: 0, 20, 40 µmol m-2 s-1 Photoperiod: 8:16, 12:12, 16:8 h L:D | Guzmán-Urióstegui and Robledo 1999 |
| G. lemaneiformis | Tetrasporophyte | Spontaneous | 20℃, 30 µmol m-2 s-1, 12:12 h L:D | Ye et al. 2006 |
| G. dura | Carposporophyte | Spontaneous | 24℃, 15 µmol m-2 s-1, 12:12 h L:D | Mantri et al. 2009 |
| G. verrucosa |
Tetrasporophyte Carposporophyte | Spontaneous | No data | Oza et al. 1994 |
| G. verrucosa |
Tetrasporophyte Carposporophyte | Spontaneous in dark Desiccation Osmotic shock (distilled water) | No data | Kim et al. 2001 |
| G. verrucosa | Carposporophyte |
Osmotic shock (tap water) | No data | Alveal et al. 1997 |
| G. arcuate var. arcuate G. corticate var. cyclindrica |
Tetrasporophyte Carposporophyte | Spontaneous | 10 µmol m-2 s-1, 8:16 h L:D | Kaliaperumal et al. 1986 |
본 연구에서 한천원료인 홍조류 꼬시래기의 과포자 방출은 물기를 제거한 엽체를 저온(5℃)의 암조건에서 2 h 동안 전처리하였다가 멸균해수에 넣으면 4일 후에 대량으로 포자가 방출됨을 확인하였다. 홍조류 우뭇가사리류(Gelidium lingulatum, G. chilense)와 Gracilariopsis lemaneiformis의 포자방출은 해수에 엽체가 잠긴 자연방출(spontaneous discharge) 상태에서 환경 조건(온도, 광도, 염분, 광주기 등)을 다르게 하여 수행되었으며(Correa et al. 1985; Zhou et al. 2013), 포자방출의 최적 환경은 종별 및 생활사단계별 차이를 보였다(Table 3). Le Gall et al. (2004)는 홍조류 Palmaria palmata의 성숙한 사분포자체에서 포자를 대량 방출 받기 위하여 해수가 없는 상태로 암조건에서 하루 밤 동안 저온(4℃)에서 보관한 후 여과 해수에 넣고 폭기하면 1시간 내에 방출한다고 하였다. 본 연구를 통하여 꼬시래기의 대량 해면양식을 위한 종묘생산용 과포자 획득을 위한 최적 환경조건을 파악하였으며, 향후 포자 착생 후 최적 생장을 위한 환경 조건에 대한 연구가 필요할 것으로 판단된다.
Table 3.
Sporulation experimental conditions of red macroalgal species
| Species | Life stage |
Pretreatment condition | Culture condition | References |
| Gelidium lingulatum Gelidium chilense |
Tetrasporophyte Tetrasporophyte |
Spontaneous Spontaneous |
15℃, < 10 µmol m-2 s-1 15℃, < 10 µmol m-2 s-1 | Correa et al. 1985 |
| Gracilariopsis lemaneiformis |
Tetrasporophyte Carposporophyte |
Spontaneous Spontaneous |
Temperature: 15, 20, 25, 30℃ Irradiance: 15, 30, 45, 60 µmol m-2 s-1 Salinity: 20, 25, 30, 35 psu Photoperiod: 8:16, 12:12, 10:14, 14:10 h L:D Temperature: 15, 20, 25, 30℃ Irradiance: 15, 30, 45, 60 µmol m-2 s-1 Salinity: 20, 25, 30, 35 psu Photoperiod: 8:16, 12:12, 10:14, 14:10 h L:D | Zhou et al. 2013 |
| Palmaria palmata | Tetrasporophyte |
Low temp. (4℃) × Desiccation (overnight) | No comparison | Le Gall et al. 2004 |