1. 서 론
꼬시래기류(Gracilarialean red algae)는 식용 한천과 샐러드 원료로서 경제적 가치가 높으며(Zemke-White and Ohno 1999; Polifrone et al. 2006), 우리나라에서는 70년대 초반부터 해면 양식되는 종이다(Shang 1976; Kain and Destombe 1995; Buschmann et al. 2001). 현재 꼬시래기류 양식은 엽체 일부를 양식줄에서 생장시켜 수확하는 영양체 채묘방법이 주로 이용되는데, 이는 노동-집약적이며, 양식 종묘 확보를 위한 다량 채집으로 인한 야외개체군의 생물량 감소에 대한 문제점이 야기되고 있다(Jayasankar and Varghese 2002). 따라서, 꼬시래기의 사분포자(tetraspore)와 과포자(carpospore)를 이용한 포자채묘방법이 효율적인 대안으로 지속적인 관심이 증가되고 있다(Alveal et al. 1997; Guzmán-Urióstegui and Robledo 1999; Michetti et al. 2013). 특히, 꼬시래기류의 낭과는 육안으로 성숙상태가 확인가능하고 소량의 과포자체에서 과포자를 대량 확보할 수 있어 일부종의 양식에 포자채묘방법이 사용되고 있다(Glenn et al. 1996).
북반구의 온대해역에서 꼬시래기(Agarophyton vermiculophyllum)의 과포자체 출현은 여름철과 가을철에 한정되어 확보할 수 있기 때문에(Kim et al. 1998, 2001), 겨울철에 성숙한 사분포자체의 사분포자를 이용한 종묘생산 기술을 개발하기 위해서는 사분포자체(과포자 유래)와 배우체(사분포자 유래) 유배의 생장에 미치는 환경요인의 영향을 파악하는 등 생리적 연구가 매우 중요하다(Guillemin et al. 2013). 더구나, 꼬시래기류는 세대별(사분포자체와 배우체 세대)과 발생단계별(현미경적 배아단계, 육안적 유배단계)에 따라 생존과 생장 차이가 있으므로 과포자와 사분포자 배아 생장 실험은 종묘생산을 위하여 필요한 연구이다(Guillemin et al. 2013). Yokoya et al. (1999)은 꼬시래기(A. vermiculophyllum) 성체에 대한 생장실험에서 배우체는 20–30°C에서, 사분포자체는 15–25°C에서 최대 생장함을 확인함으로써 최적 생장온도가 생활사에 따라 다르다고 보고하였다. 본 연구의 목적은 한천 원료인 꼬시래기의 생활사 단계에서 사분포자체(과포자 유래, 2n)와 배우체(사분포자 유래, n)가 기질에 부착한 후 일어나는 초기생장 단계인 원반형 부착기(discoid holdfast)와 직립형 유배(erect sporeling) 생장에서 온도와 광도의 영향을 파악하여 포자채묘방법의 양식기술에 대한 기초자료를 확보하는데 있다.
2. 재료 및 방법
꼬시래기의 사분포자체(2n, 과포자 유래)와 배우체(n, 사분포자 유래)의 초기 생장에 온도와 광도가 미치는 영향을 파악하기 위하여, 충남 보령군 무창포(36º24´N, 126º53´E) 해안에서 2016년 9월에 낭과를 가진 암배우체를, 그리고 2016년 12월에 성숙한 사분포자체를 채집하였다. 실험실로 운반한 엽체는 해부현미경하에서 멸균해수와 유화용 붓으로 수회 세척되었고 건조·저온 충격(desiccation and low-temperature shock)으로 전처리한 후에 25°C, 60 µmol photons m-2 s-1와 16:8 h L:D 광주기로 세팅된 배양기에서 방출된 과포자와 사분포자를 확보하였다. 건조·저온 충격은 성숙한 꼬시래기의 엽체 표면에 있는 해수를 페이퍼 타올로 제거하고 호일로 광을 차단한 후 5°C의 배양기에서 2 h 동안 보관하였다.
꼬시래기의 과포자와 사분포자 현탁액(15 mL)을 슬라이드글라스 조각(1 × 1 cm)과 PES 배양액(Provasoli 1968) 10 mL이 담긴 Petri dish (Ø, 5 cm; H, 1.5 cm)에 접종한 후, 생장 실험은 동일한 광주기 12:12h L:D의 4가지 다른 온도(20, 25, 30, 35°C) 및 3가지 다른 광도(20, 60, 100 µmol photons m-2 s-1)에서 수행되었다. 배양기의 광원은 형광등이었으며, 20 µmol photons m-2 s-1의 광도는 검은색 망으로 Petri dish를 덮어 확보하였으며, 광도 60과 100 µmol photons m-2 s-1는 형광등과 Petri dish의 간격을 조절하여 만들었다. 온도와 광도의 조합 실험구(총 12가지)별 생장실험을 3회 반복하였으며 배양액은 3일 간격으로 전량 교환하였다.
슬라이드 조각에 착생한 사분포자체와 배우체는 다세포성 원반형 부착기(discoid holdfast)로 생장하였고, 25°C 와 100 µmol photons m-2 s-1의 배양조건에서는 배양 14일 후부터 원반형 부착기의 가운데 부위에서 직립형 유배(erect sporelings)가 형성되기 시작하였다. 각 온도 × 광도 실험구에서 사분포자체와 배우체의 원반형 부착기들은 광학현미경에 부착된 디지털카메라로 촬영하였다. 원반형 부착기 단계의 배아 중에서 근처의 다른 배아와 융합(coalescence)이 일어나지 않고 직립형 유배가 형성되지 않은 30개체를 무작위로 선택하여 Image J 프로그램으로 면적을 측정하였고, 상대생장률(RGR, relative growth rate)을 아래의 식으로 계산하였다(Serisawa et al. 2002).
RGR (% day-1) = 100 (ln A2 – ln A1)/T2–T1
A2는 배양 종료 시 원반형 부착기 면적, A1은 배양 개시 때의 포자 면적, T2–T1는 배양일 수(day)를 나타낸다.
실내배양에서 생장한 꼬시래기 사분포자체와 배우체의 원반형 부착기에서 생성된 직립형 유배(유배로 통일함)를 유화용 붓으로 조심스럽게 분리시킨 후 Petri dish에 모았다. 생활사 단계별(사분포자체, 배우체) 유배 5개체와 PES 배지(15 mL)가 담긴 36개의 Petri dish를 준비하였다(총 180개 유배). 이들은 4개 온도(20, 25, 30, 35°C)에 9개체씩 할당하였고, 3개의 광도(20, 60, 100 µmol photons m-2 s-1)에서 14일 동안 배양한 후 길이를 측정하여 상대생장률을 계산하였다. 실험구별 3개의 반복구를 두었으며 배양액은 3일 간격으로 전량 교환하였다.
3. 통계분석
꼬시래기의 사분포자체와 배우체의 원반형 부착기 생장과 유배 생장에 온도와 광도의 영향을 파악하기 위하여 통계분석을 실시하였다. 먼저, 데이터의 동질성을 확인하기 위하여 등분산검정(homogeneity of variances)을 Cochran’s test로 실시하였으며, 사분포자체와 배우체의 원반형 부착기 생장과 유배 생장에 대한 온도와 광도의 영향은 two–way ANOVA로 유의차를 검정하였다. 평균에 대한 유의차가 발견되면 Tukey’s HSD test 방법으로 사후 검정하였으며(Sokal and Rohlf 1995), 데이터 분석을 위해 사용한 통계 프로그램은 STATISTICA version 5.0 이다.
4. 결 과
원반형 부착기 생장
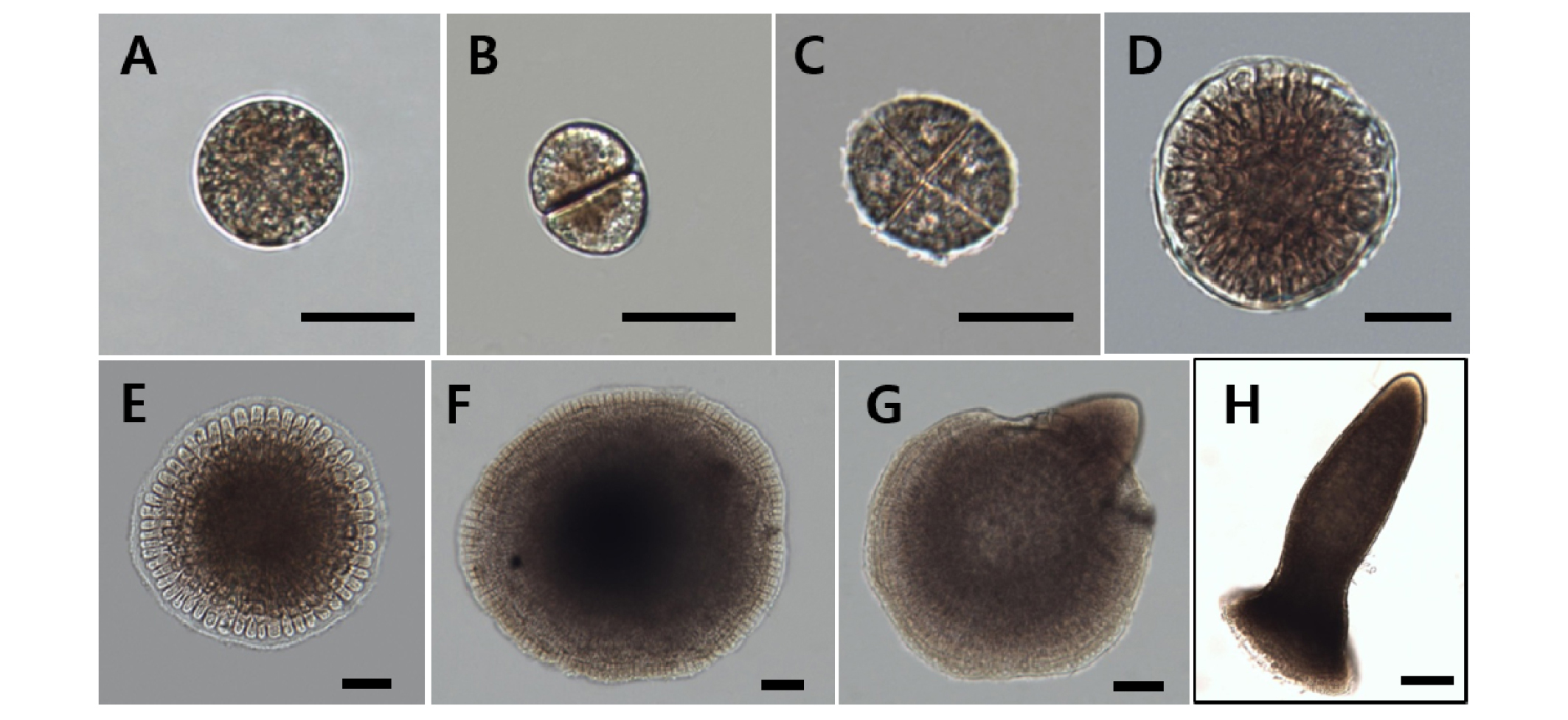
꼬시래기의 과포자와 사분포자는 착생 1일 이내에 슬라이드글라스 조각의 표면에 착생한 후 사분포자체와 배우체의 원반형 부착기(Fig. 1A~F)와 직립형 유배(Fig. 1G~ H)로 생장하였다. 착생 1일 후, 사분포자체 부착기의 면적은 881.25±35.79 ㎛2 (mean±SE, n = 30 spores)였으며, 직경은 32.94±0.87 µm (n = 30)이였다. 배양 14일 후, 원반형 부착기의 면적은 2,465.43–47,301.76 ㎛2였고 상대생장률은 7.08–28.38% day-1였다. 사분포자체의 부착기는 30°C의 100 µmol photons m-2 s-1에서 최대생장을 보였으며, 35°C에서도 생장률이 7.08–23.28% day-1로서 빠른 생장을 보였다(Fig. 2A).
사분포자에서 자란 배우체의 원반형 부착기 면적은 착생 1일 후 869.23±24.35 ㎛2 (n = 30 spores)였으며, 직경은 33.37±0.79 µm (n = 30)로 확인되었다. 배우체의 원반형 부착기는 35°C 에서 배양 7일부터 50%이상 탈색되었으며, 14일 후에는 모든 원반형 부착기는 탈색 및 사멸되었다. 배양 14일 후, 20–35°C에서 부착기 면적은 4,421.60–24,198.91 ㎛2로 증가하였으며, 상대생장률은 11.58–23.67% day-1였다. 배우체는 25°C의 100 µmol photons m-2 s-1에서 최대생장을 보였으며, 30°C의 20 µmol photons m-2 s-1에서 느린 생장을 보였다(Fig. 2B).
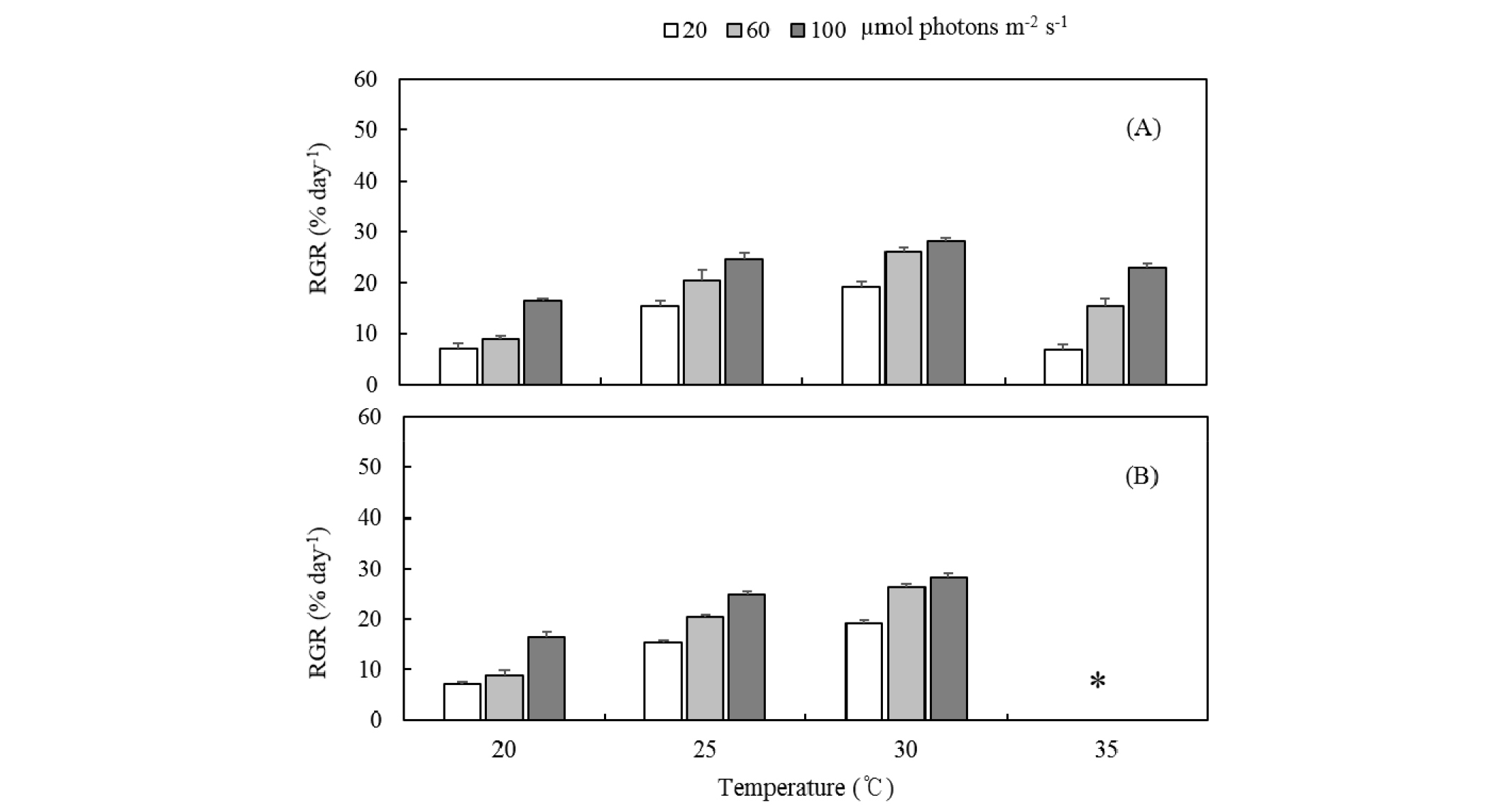
Fig. 2.
Relative growth rates (RGRs) of discoid holdfasts of Agarophyton vermiculophyllum. (A) Tetrasporophytes (2n) germinated from carpospores, (B) Gametophytes (n) germinated from tetraspores. They were cultured under combinations of three irradiance and four temperature levels for 14 days. Photoperiod was same with 12:12h L:D. Vertical bars indicate mean±SE (n = 3 replicates). *, discoid holdfast death
원반형 부착기 단계에서 사분포자체는 20–35°C에서, 그리고 배우체는 20–30°C에서 광도(20, 60, 100 µmol photons m-2 s-1)가 증가할 때 생장은 촉진되었다. 특히, 배우체는 35°C의 모든 광도에서 사멸하였으나, 사분포자체가 생존 및 생장이 가능하여 배우체에 비해 고온 내성이 강한 것으로 확인되었다. 사분포자체와 배우체의 원반부착기의 생장은 온도별(p < 0.001)과 광도별(p < 0.001)로 유의한 차이를 보였다(Table 1).
Table 1.
Analysis of variance (two-way ANOVA) for the effects of temperature and irradiance on the relative growth rate (RGR, % day-1) of holdfast areas in the tetrasporophyte and gametophyte stages of Agarophyton vermiculophyllum after 14 days in culture
Tukey HSD test 결과, 사분포자체의 원반형 부착기 생장은 20°C과 35°C에 비해 30°C에서 빠른 생장을 보였으나(p < 0.05), 25°C에서 부착기 생장은 30°C, 그리고 35°C와 유의한 차이가 없었다. 사분포자체 원반형 부착기 생장은 100 µmol photons m-2 s-1에서 최대로서 20 µmol photons m-2 s-1에 비해 빠른 생장을 보였으나 (p < 0.05), 다른 광도별 생장 차이는 없는 것으로 나타났다(p > 0.05). 배우체의 원반형 부착기 생장은 20°C와 30°C에서 유의한 차이가 없었으나, 25°C에 비해 느린 생장을 보였다(Tukey test, p < 0.05). 또한, 배우체의 원반형 부착기 생장은 광도별(20, 60, 100 µmol photons m-2 s-1)로 유의한 차이를 보였으며, 100 µmol photons m-2 s-1에서 최대였고 20 µmol photons m-2 s-1에서 최소였다(p < 0.05).
직립형 유배 생장
꼬시래기의 사분포자체와 배우체 유배는 다양한 온도(20–35°C)와, 광도(20–100 µmol photons m-2 s-1)에서 생장하였다. 배양 개시 전에 사분포자체 유배 길이는 평균 1.96±0.03 mm (n = 30 individuals)였으며, 배양 14일 후에 2.96–9.62 mm로 생장하였다. 사분포자체 유배의 상대생장률은 2.93–11.11% day-1로서 25°C의 60 µmol photons m-2 s-1에서 최대였고(Fig. 3A), 온도에 의한 유의차는 확인되었으나, 광도 혹은 온도와 광도 조합에서는 생장에 대한 유의차가 나타나지 않았다(Table 2).
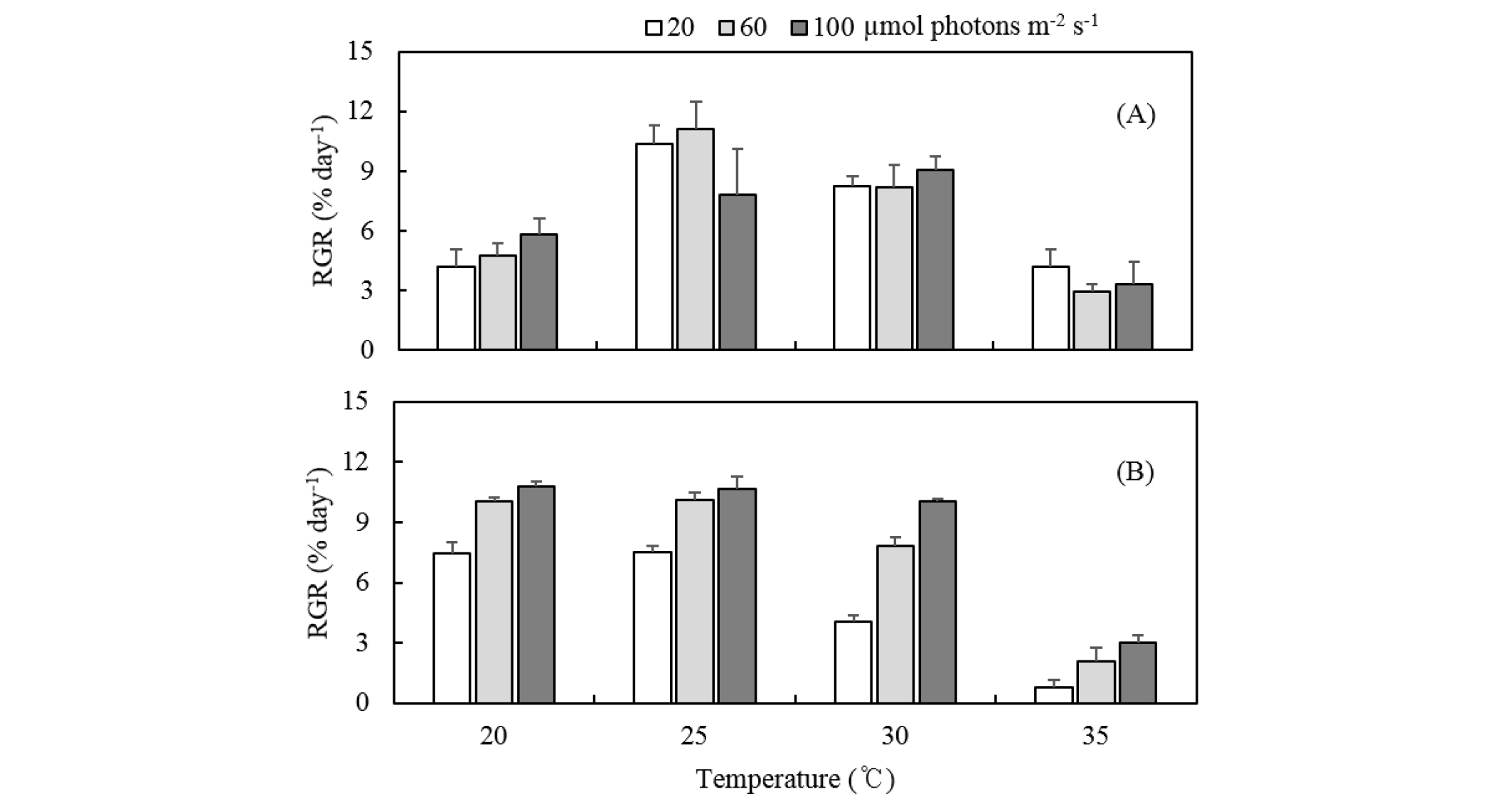
Fig. 3.
Relative growth rates (RGRs) of erect thallus of Agarophyton vermiculophyllum. (A) Tetrasporophytes (2n), (B) Gametophytes (n). They were cultured for 14 days under combinations of three irradiance and four temperature levels. Photoperiod was same with 12:12h L:D. Vertical bars indicate mean±SE (n = 3 replicates)
Table 2.
Analysis of variance (two-way ANOVA) for the effects of temperature and irradiance on the relative growth rate (RGR, % day-1) of juvenile lengths in the tetrasporophyte and gametophyte stages of Agarophyton vermiculophyllum after 14 days in culture
배우체 유배는 배양 개시 전에 평균 2.20±0.13 mm (n = 30)였으며, 14일 후 길이 2.47–10.04 mm로 생장하였고 이때 상대생장률은 0.78–10.82% day-1였으며 20°C의 100 µmol photons m-2 s-1에서 최대 생장을 보였다(Fig. 3B). 온도와 광도는 꼬시래기 배우체 유배의 생장에 영향을 미치는 것으로 확인되었으며, 온도와 광도의 상호작용도 영향을 주는 것으로 나타났다(Table 2).
5. 고 찰
꼬시래기류(Gracilaria spp.)의 과포자와 사분포자는 기질에 부착한 후 원반형 단계, 부착기 형성 단계, 그리고 직립 유배 형성 단계의 순서로 분화한다(Orduña-Rojas and Robledo 1999; Mantri et al. 2009; Michetti et al. 2013). Gracilaria chilensis와 G. dura의 포자채묘(spore seeding)에서 포자의 분화패턴에 대한 연구(원반형 분화, 부착기 발달 등)는 외해양식을 위해서 필수적인 부분이다(Alveal et al. 1997; Mantri et al. 2009). Gracilaria dura의 포자가 부착한 후 생장한 원반형 부착기(discoid holdfast)에서 직립형 유배가 형성되는 기간은 15–20일로 확인되었으며, G. cornea는 21일 배양 후에 직립형 유배가 생성되었다(Orduña-Rojas and Robledo 1999). 본 연구에서 A. vermiculophyllum의 직립형 유배는 최적 생장 온도(25°C)와 광도(100 µmol photons m-2 s-1) 조건에서 포자를 접종하고 14일이 경과한 후에 관찰되었으며, 과포자와 사분포자의 분화패턴과 직립형 유배가 형성되는데 걸리는 기간은 유사하였다.
Guillemin et al. (2013)은 G. chilensis의 부착기생장(holdfast growth)은 낮은 광도(20 µmol photons m-2 s-1)에서는 15 psu와 35 psu의 모든 조건에서 배우체가 포자체에 비해 빠른 생장을 보였으나, 반대로 고광도(60 µmol photons m-2 s-1)에서는 사분포자체가 배우체에 비해 빠른 생장을 보임으로써 배우체와 사분포자체의 부착기 생장은 광도에 따라 다름을 증명하였다. 본 연구 결과, 무창포 꼬시래기(A. vermiculophyllum)의 사분포자체와 배우체의 원반형 부착기의 상대생장률은 실험 온도(20, 25, 30°C)와 광도(20, 60, 100 µmol photons m-2 s-1)의 조합조건에서는 온도와 광도의 증가에 비례하였으며, 35 °C에서는 모든 광도에서 배우체(n)가 사멸하였으나, 사분포자체(2n)는 생장함으로써 사분포자체의 고온내성을 제시한다. 한국의 서해안 무창포 해안에서 꼬시래기는 여름철에 성숙한 낭과를 가진 암배우체에서 과포자를 방출하므로 수온이 높은 여름–초가을에 과포자가 착생하여 사분포자체(2n)로 생장한다. 따라서 본 연구에서 사용한 사분포자체의 원반형 부착기는 35°C에서 생장이 잘되지만, 수온이 낮은 가을–봄에 성숙하여 방출된 사분포자가 착생하여 생장한 겨울철 배우체(n)의 원반형 부착기의 생장은 높은 수온에 적응이 되지 않아서 35°C에서 모두 사멸한 것으로 사료된다. 따라서, 국내산 꼬시래기의 과포자 채묘는 원반형 부착기 생장이 좋은 높은 온도와 광도의 여름철에 수행되는 것이 적합한 것으로 확인되었다.
본 연구에서 꼬시래기의 사분포자체(2n)의 원반형 부착기 생장은 30°C의 100 µmol photons m-2 s-1에서 28.19% day-1(상대 생장률)로 최대였으며, 배우체(n)는 25°C의 100 µmol photons m-2 s-1에서 최대(23.52% day-1)를 보였다. 또한, 꼬시래기의 사분포자체 유배의 상대생장률은 25°C의 60 µmol photons m-2 s-1에서 11.11% day-1로 최대였고, 배우체 유배는 20°C의 100 µmol photons m-2 s-1에서 10.82% day-1로서 최대였다. Orduña-Rojas and Robledo (1999)는 Gracilaria cornea를 다양한 온도(25, 28, 31°C)와 광도(10, 25, 50, 75, 100 µmol photons m-2 s-1)의 조합조건에서 8주 동안 실내 배양하였을 때 최대 상대생장률 5.20% day-1를 제시하였다. 본 연구 결과, 꼬시래기는 G. cornea에 비해 높은 상대생장률을 보였고 사분포자체의 원반형 부착기와 유배는 배우체에 비해 고온에서도 높은 상대생장률을 보였으며, 발생 단계(원반형 부착기, 유배)에 따라 생장을 위한 최적온도와 광도 및 생장률에서 차이가 있음을 확인할 수 있었다.
결론적으로 꼬시래기 유배의 상대생장률은 11.11% day-1로 해외에서 해면양식 중인 Gracilaria cornea (5.20% day-1)와 G. dura의 4.67% day-1 (Mantri et al. 2009)에 비해 2배 이상 높게 나타남으로써 해면양식이 가능할 것으로 사료된다. 또한, 꼬시래기 야외개체군의 생물량과 유전적 다양성(genetic diversity)을 증가시키기 위해서는 향후 고온 내성과 생장이 빠른 과포자를 이용한 포자채묘 기술 개발에 대한 더 많은 연구가 필요한 실정이다.