1. 서 론
2. 재료 및 방법
시료추출 및 분획
세포배양
DPPH radical 소거 활성
Peroxynitrite 소거 활성
Ferric reducing antioxidant power (FRAP) 측정
MTT assay를 이용한 세포생존율 측정
세포내 활성 산소종(ROS) 측정
Genomic DNA의 추출 및 산화 생성물 측정
총 polyphenol 함량 측정
총 flavonoid 함량 측정
NO 생성 억제 효과
mRNA 추출과 RT-PCR (reverse transcription-polymerase chain reaction)
통계처리
3. 결과 및 고찰
DPPH radical 소거활성
Peroxynitrite 소거 활성
Ferric reducing antioxidant power (FRAP) 측정
세포내 ROS 소거 활성
Genomic DNA의 산화억제 활성 측정
총 폴리페놀과 총 플라보노이드 함량 분석
NO 생성 억제능 측정
IL-1β, IL-6 및 COX-2의 mRNA 유전자 발현 저해효과
4. 결 론
1. 서 론
세포의 미토콘드리아는 생명을 유지하기 위해 필수적인 에너지인 ATP를 생성하는 기관으로, 대사 과정 중 세포 내 산소 대사를 통해 초과산화물 라디칼(superoxide radical), 하이드록실 라디칼(hydroxyl radical), 과산화수소 등 반응성이 큰 활성산소종(reactive oxygen species)을 생성하게 된다. 이들 활성산소종은 인체 내에서 세포내 지질, 단백질 및 DNA를 손상시키고 정상적인 기능을 방해하여 세포 노화를 촉진시킨다. 인체는 이들 활성산소종의 생성을 차단시키거나 생성된 활성산소종을 제거하기 위한 항산화 시스템을 가지고 있어, 정상적인 상태에서는 활성산소종의 산화작용이 생체 항산화 시스템에 의해 방어되기 때문에 해로운 영향을 미치기 힘들다. 그러나 환경의 변화나 질병 등 항산화 능력의 평형이 깨지게 되면 산화스트레스가 발생하게 된다(Lee et al. 2011; Lee and Park 2020).
이와 같은 과량의 ROS로 인한 산화적 스트레스가 항산화물질에 의해 감소되는 것이 알려지면서 항산화 물질을 개발하기 위한 연구들이 지속적으로 이루어지고 있다. 현재 상업적으로 사용되고 있는 합성 항산화제는 탁월한 효과와 경제성 때문에 많이 사용되고 있지만 인체에 대한 안전성 문제로 천연 항산화제에 관심이 쏠리고 있다. 특히 과일이나 채소를 적절히 섭취하면 거기에 포함된 항산화 성분이 신체의 항산화능의 균형을 유지시켜 줄 수 있다는 것이 보고됨에 따라 천연물유래 항산화 소재에 관한 연구가 활발히 진행되고 있다(Williams et al. 1990; Jayaprakasha et al. 2003).
인체의 염증반응은 인체의 생체조직을 방어하기 위한 기전으로 염증반응에 관여하는 대표적인 세포 중 하나인 대식세포는 interleukin (IL)-6, IL-1β 등과 같은 염증 촉진성 사이토카인(pro-inflammatory cytokine)과 일산화질소(NO), 유도성 질소산화물 합성효소(iNOS), cyclooxygenase -2(COX-2) 등의 염증유발인자들을 생성한다. 활성산소의 하나인 NO는 세균을 죽이거나 종양을 제거하는 중요한 역할을 하지만 외부요인에 의해 과도한 NO가 생성될 경우 염증을 유발시켜 생체 조직 손상이나 유전자 변이 등 다양한 병리학적 기전에 관여한다고 알려져 있다(Mc Cartney-Francis et al. 1993; Seibert et al. 1994; Storck et al. 1994). 이러한 만성 염증 질환의 치료를 위해 합성 항염증제가 사용되고는 있으나 부작용의 우려가 있어 보다 안전한 항산화 및 항염증 효과가 있는 천연물 유래 소재의 개발이 중요시 되고 있다
본 연구팀에서는 우리나라의 염생식물 시료로부터 항산화 활성을 스크리닝하는 과정에서 도깨비고비 추출물이 HT-1080 세포내에 발생하는 산소활성종(ROS)에 대한 소거활성이 있음을 확인하였다. 염생식물인 도깨비고비(C. falcatum)는 한국, 일본 및 타이완 등지에서 자생하는 양치식물이다. 다른 이름으로는 ‘도깨비쇠고비’, ‘긴잎도깨비고비’라고도 하며, 바닷가와 섬의 바위틈에서 자란다. 이 식물의 뿌리줄기와 잎자루는 이전부터 해열과 지혈작용 및 회충구제 등에 약용으로 사용되었으며 여기로부터 몇 개의 플라보노이드가 분리된 바 있으나, 이 식물의 생리활성에 대한 연구는 전혀 보고되지 않았다(Iwashina et al. 2006; 한국학중앙연구원 2017). 따라서 본 연구에서는 도깨비고비의 추출물 및 그 용매 분획물을 제조하여 DPPH (1,1-diphenyl-2- picrylhydrazyl)와 peroxynitrite 소거능, 세포내 ROS 소거능 및 DNA 산화억제 등에 대한 항산화 활성과 LPS로 염증을 유도한 RAW 264.7 대식세포에서 NO 생성 억제와 염증관련 인자의 발현에 미치는 영향을 검토하여 도깨비고비의 항산화 및 항염증 소재로서의 이용 가능성을 탐색하고자 하였다.
2. 재료 및 방법
시료추출 및 분획
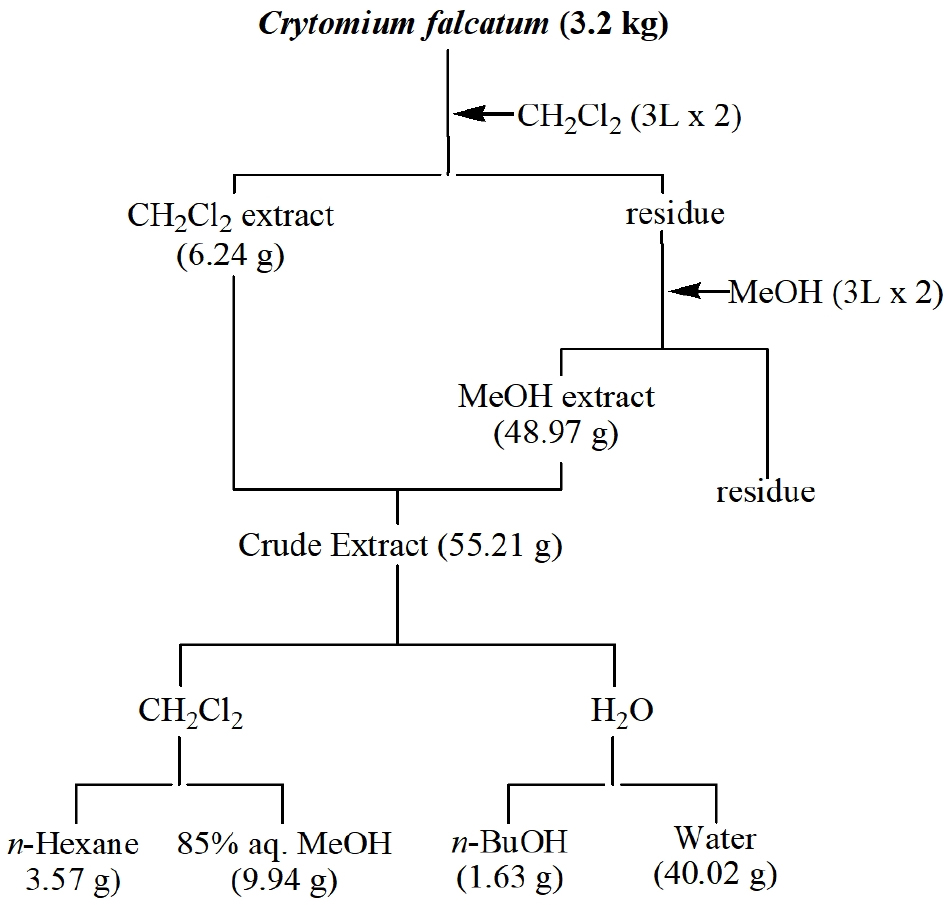
실험에 사용된 도깨비고비(C. falcatum)는 2019년 9월 제주도 표선면에서 채집하였다. 응달에서 건조한 도깨비고비 시료(3.2 kg)를 추출에 용이하게 세절한 후 methylene chloride (CH2Cl2)에 24시간 침지한 후 여과하여 1차 CH2Cl2 추출액을 얻었으며, 이 과정을 다시 반복하여 2차 CH2Cl2 추출액을 얻었다. 1차와 2차 CH2Cl2 추출액을 합하여 회전진공증발기로 용매를 제거한 후에 6.24 g의 추출물을 얻었다. 여과하고 남은 시료에 동량의 methanol (MeOH)을 사용하여 시료를 침지시켰고 동일한 방법으로 반복 추출하여 MeOH 추출물 48.97 g을 얻었다. 이 두 추출물을 혼합하여 추출물(crude extract) 55.21 g을 얻었다. 혼합한 추출물은 CH2Cl2와 물을 사용하여 1차 용매분획을 진행하였다. CH2Cl2 분획 층은 농축하여 n-hexane과 85% aq.MeOH로 재분획하였고, 물 층은 n-BuOH을 첨가하여 n-BuOH과 물 분획 층으로 재분획하였다. 각 분획 층의 용매를 제거한 후에 n-hexane, 85% aq.MeOH, n-BuOH 및 물 분획 층이 각각 3.57 g, 9.94 g, 1.63 g, 40.02 g이 얻어졌다(Fig. 1).
세포배양
실험에 사용한 HT-1080과 Raw 264.7 세포주는 한국세포주은행으로부터 분양받아 사용하였다. 사용한 배지는 RPMI-1640 배지에 100 units/ml의 penicillin-streptomycin과 10% FBS (fetal bovine serum)를 첨가한 배지를 사용하였다. 세포를 배양한 incubator의 배양조건은 37°C, 5% CO2의 조건에서 배양하였으며, 배양한 세포는 각각 일주일에 2~3회 1X PBS buffer를 사용하여 세척한 후 배지를 교환하였고, 0.05% trypsin-0.02% EDTA solution을 사용하여 부착된 세포를 분리하여 계대배양하였다.
DPPH radical 소거 활성
DPPH (1,1-diphenyl-2-picrylhydrazyl) 시약 2 mg 을 ethanol (EtOH) 15 ml에 녹여 만든 DPPH원액 1.2 ml와 3 ml의 EtOH, 0.5 ml의 dimethyl sulfoxide (DMSO)를 같은 비율로 혼합하여 DPPH radical solution을 준비한다. 준비된 DPPH radical solution을 cuvette에 넣고 518 nm의 파장에서 흡광도를 측정하여 그 측정값이 0.95~0.98이 되도록 농도를 조절하였다. 농도를 조절한 DPPH radical solution 900 μl에 준비한 시료 100 μl를 가하여 vortex한 후 10분 후에 518 nm의 파장에서 흡광도를 측정하였다(Blois 1958).
Peroxynitrite 소거 활성
Peroxynitrite (ONOO-) 소거 활성은 dihydrorhodamine 123(DHR 123)의 산화되는 정도를 측정하여 나타내었다. DHR 123은 dimethylformamide (DMF)에 녹여 질소로 purge시켜 -80°C 에 보관하였다. Rhodamine buffer는 90 mM sodium phosphate, 90 mM sodium chloride, 5 mM potassium chloride를 혼합하여 pH를 7.4로 조절한 뒤 100 μM diethylentriaminepenta acetic acid (DTPA)를 혼합하여 냉장 보관하였고, buffer로 DHR 123을 5 μM로 희석하여 실험에 사용하였다. DHR 123 buffer 용액에 화합물과 peroxynitrite를 첨가하고 실온에서 5분간 방치 후, Victor3 1402 multilabel counter를 이용하여 excitation 485 nm, emission 530 nm에서 측정하였다. Authentic peroxynitrite 대신에 SIN-1을 첨가하는 경우는 동일한 방법으로 실시하여 1시간동안 방치한 후 측정하였다. 이는 SIN-1이 NO·와 O2·-를 동시에 발생시켜 ONOO-를 생성시키는 화합물로, authentic peroxynitrite의 급속한 DHR 123의 산화와는 달리 점진적으로 산화가 일어나기 때문이다. 공실험(blank)은 0.3 N NaOH를 사용하였고, 실험은 3회 반복하였으며, 결과는 blank를 차감한 값을 평균하여 대조군에 대한 백분율로 계산하였다(Kooy et al. 1994).
Ferric reducing antioxidant power (FRAP) 측정
Ferric reducing antioxidant power (FRAP) assay를 통해 항산화 능력을 알아보았다. 200 mM의 sodium phosphate buffer 200 μl에 농도별로 희석한 도깨비고비 추출물 및 용매 분획물 200 μl와 1% potassium ferricyanide 200 μl를 첨가하여 이 혼합물을 50°C에서 20분간 반응시킨다. 반응물에 10% trichloroacetic acid 200 μl를 첨가한 후 10,000 rpm에서 10분간 원심분리를 하여 상등액을 취한다. 취한 상등액 500 μl에 0.1% ferric chloride 500 μl를 첨가하여 700 nm에 측정하여 값을 나타낸다. 대조군으로는 ascorbic acid (vitamin C)를 사용하여 비교한다(Oyaizu 1986).
MTT assay를 이용한 세포생존율 측정
도깨비고비의 추출물 및 용매 분획물에 대한 세포 증식 억제 효과를 확인하기 위하여 MTT [3-(4,5-dimethylthiazol -2-yl)-2,5-diphenyl tetrazolium bromide] 시약을 이용하여 HT-1080 세포에 대한 세포독성을 측정하였다. 배양된 HT-1080 세포는 4 × 103 cells/well이 되도록 96 well plate에 분주하여 37°C, 5% CO2 incubator에서 24시간 동안 배양하였다. 새 배지로 교체한 뒤 농도별로 준비한 시료를 처리한 후 다시 1시간 동안 배양하였다. 시료를 처리한 후 배양된 세포에 1 mg/ml의 MTT 시약을 처리하여 4시간 동안 배양하여 formazan이 형성되는 것을 확인하고, MTT시약이 처리된 배지를 제거한 후 형성된 formazan을 DMSO에 녹여 Victor3 multilabel plate reader를 이용해 540 nm에서 흡광도를 측정하여 세포생존율을 구하였다. 세포 생존율이 80% 이상인 농도를 최고 농도로 하여 세포 실험을 진행하였다.
세포내 활성 산소종(ROS) 측정
세포내 ROS free radical 생성은 DCFH-DA assay로 측정하였다. HT-1080 세포를 96 well plate에 3 × 105 cells/well이 되도록 분주하였고, 37°C, 5% CO2 incubator에서 24시간 배양하였다. 배양된 세포는 PBS로 씻은 후 20 μM DCFH-DA를 각 well에 처리하여 다시 37°C, 5% CO2 incubator에서 20분간 pre-incubation하였다. 각각의 well에 농도별로 준비한 시료를 처리하여 37°C, 5% CO2 incubator에서 1시간 동안 incubation한 후, DCFH-DA를 제거하고 PBS로 washing 후 500 μM H2O2를 처리하여 시간별로 DCF fluorescence를 excitation 485 nm, emission 530 nm에서 Victor3 1402 multilabel counter로 측정하였다(Okimoto et al. 2000).
Genomic DNA의 추출 및 산화 생성물 측정
도깨비고비의 추출물 및 용매 분획물이 genomic DNA의 산화정도를 방어한 정도를 측정하였다. 실험에 사용한 genomic DNA는 AccuPrep® Genomic DNA Extraction kit (Bioneer Inc., USA)를 이용하여 HT-1080 세포로부터 추출하였다. 추출한 genomic DNA는 260 nm와 280 nm의 파장에서 그 흡광도를 측정하여 각각의 순도와 농도를 정량한 후, -20°C에서 냉동보관하여 사용하였다. 0.5~1.0 μg의 genomic DNA에 4 μl의 DEPC-DW와 600 μM의 FeSO4, 0.5 mM의 H2O2를 각각 10 μl씩 가하여 genomic DNA를 30분간 상온에서 산화시킨 뒤, 130 mM의 EDTA를 가하여 반응을 중지시켰다. 산화된 genomic DNA는 6X agarose gel loading buffer와 혼합한 후 1% agarose gel에 loading하여 100 mV로 전기영동하였다. 전기영동을 마친 gel은 5 μg/ml EtBr에 20~30분간 염색시켜 UV를 통해 산화된 정도를 확인하고 사용된 시약의 농도와 양을 조절하여 실험하였다(Milne et al. 1993).
총 polyphenol 함량 측정
도깨비고비의 총 폴리페놀 함량 측정은 Folin-Denis 방법에 따라 진행하였다. 2배 희석한 Folin-Denis 시약 500 μl에 1 mg/ml 농도로 희석한 추출물 및 용매 분획물 500 μl를 첨가한 후 실온에서 3분간 반응한다. 그 후 Na2CO3 용액 500 μl를 첨가하여 실온에서 1시간 반응한다. 750 nm에서 흡광도를 측정하여 함량을 표시한다. 표준물질로는 tannic acid (Duksan, 경기도 안산시)를 사용하여 추출물 및 용매 분획물과 동일한 방법으로 분석하여 검량선을 얻어서 총 폴리페놀 함량을 산출하였다. 시료의 실험은 총 3회 반복하여 평균값을 표기하였다.
총 flavonoid 함량 측정
도깨비고비의 총 플라보노이드 함량을 측정하기 위하여 Lee et al. (1997)의 방법에 따라 진행하였다. 도깨비고비의 추출물 및 용매 분획물 시료 50 μl에 1 N NaOH 120 μl와 diethylene glycol 1 ml를 첨가한 후 37°C에서 1시간동안 반응한다. 이 후 420 nm에서 흡광도를 측정하여 함량을 표시한다. 표준물질로는 naringin (Sigma, USA)을 사용하였다.
NO 생성 억제 효과
Raw 264.7 세포를 96 well micro-plate에 1 × 104 cells/ml로 well당 100 μl씩 분주하여 37°C, 5% CO2 incubator에서 24시간 동안 배양하였다. 배양액을 10% FBS가 함유된 Modified Eagle Medium (MEM)으로 교체한 뒤 준비된 시료를 처리한 후 1시간 동안 배양하였다. 그 뒤, NO 생성을 유도하기 위해 1 μg/ml (1 ppm)의 LPS를 처리하여 37°C, 5% CO2 incubator에서 48시간 동안 배양하였다. LPS에 의해 자극받은 Raw 264.7세포로부터 생성된 NO가 함유된 배지 50 μl와 Griess 시약(0.1% N-1-naphtylenediamine : 1% sulfanilamide = 1 : 1) 50 μl를 반응시켜 570 nm에서 흡광도를 측정하였다(Nataliya and Andrei 2005).
mRNA 추출과 RT-PCR (reverse transcription-polymerase chain reaction)
Raw 264.7 세포를 1 × 104 cells/well이 되도록 6 well plate에 분주하였고 37°C, 5% CO2 incubator에서 24시간 배양하였다. 그 뒤 마찬가지로 상등액을 제거하고 FBS가 포함되지 않은 배지로 교체 후 농도별로 준비한 시료를 처리하였고, 1시간 뒤 염증 유도를 위해 1 ppm의 LPS를 처리하고 24시간 배양하였다. 상등액을 제거하고 남은 세포에 Trizol reagent를 첨가하여 세포로부터 RNA를 추출하였고, 분리하고 정량한 RNA 2 μg에 DEPC-treated water와 oligo dT를 첨가하여 70°C에서 5분간 denaturation 한 뒤 4°C로 유지했다. 이후 RNA에 PCR mixture (1X RT buffer, 1 mM dNTP, 500 ng oligo dT 140 U M-MLV reverse transcriptase, 40 U RNase inhibitor)를 첨가하여 42°C에서 1시간, 72°C에서 5분 동안 thermal cycler를 사용하여 reverse transcription하였다. 각각의 target DNA는 다음 sense와 antisense primer를 첨가하여 증폭시켰다: IL-1β forward 5'-GGG-CCT-CAA-AGG-AAA-GAA-TC -3', and reverse 5'-TAC-CAG-TTG-GGG-AAC-TCT-GC -3', IL-6 forward 5'-AGT-TGC-CTT-CTT-GGG-ACT-GA-3', reverse 5'-CAG-AAT-TGC-CAT-TGC-ACA-AC-3', COX-2 forward 5'-AGA-AGG-AAA-TGG-CTG-CAG-AA-3', and reverse 5'-GCT-CGG-CTT -CCA-GTA-TTG-AG-3', β-actin forward 5'-GCC-ACC-CAG-AAG-ACT-GTG-GAT-3', and reverse 5'-TGG-TCC-AGG-GTT-TCT-TAC-TCC-3'. Target DNA의 증폭 cycle은 95°C에서 45초, 60°C에서 1분, 72°C에서 45초를 1 cycle로 해서 30 cycle을 진행하였다. 합성한 DNA 산물은 1.5% agarose gel을 이용한 전기영동에서 100 mV, 30분으로 진행하여 분리하였다. 전기영동이 끝난 gel은 1 mg/ml의 EtBr solution에서 염색하여 CAS- 400SM Davinch-Chemi imagerTM을 사용하여 UV light로 현상하였다.
통계처리
도깨비고비의 각 추출물 및 용매 분획물로부터 얻은 실험 결과들을 유의성 검정을 진행하였다. 분산분석(ANOVA)를 진행한 후 p < 0.05 수준에서 Duncan's multiple range test를 시행하였고, 각각의 결과들은 평균(mean±) 표준오차로 표시하였다. 통계분석은 모두 SPSS statistics 프로그램을 사용하여 진행하였다.
3. 결과 및 고찰
DPPH radical 소거활성
도깨비고비 추출물 및 분획물의 DPPH radical 소거능력을 측정하였다. 추출물 및 분획 층의 농도는 각각 200, 100, 50 및 10 μg/ml의 농도로 실험을 진행하였고, 이들의 활성을 비교하기 위한 대조군으로는 BHT, BHA 및 vitamin C를 추출물 및 용매 분획 층과 동일한 농도로 제작하여 실험을 진행하였다. 실험 결과 추출물 및 용매분획 층 모두 대조군인 BHT, BHA 및 vitamin C에 비해 유의적인 활성을 나타내지는 못하였으나, 추출물 및 용매 분획층 만으로 비교하였을 때, n-BuOH 층이 200 μg/ml 농도에서 DPPH 라디칼에 대한 25.5%의 소거활성을 나타내었다(Fig. 2).
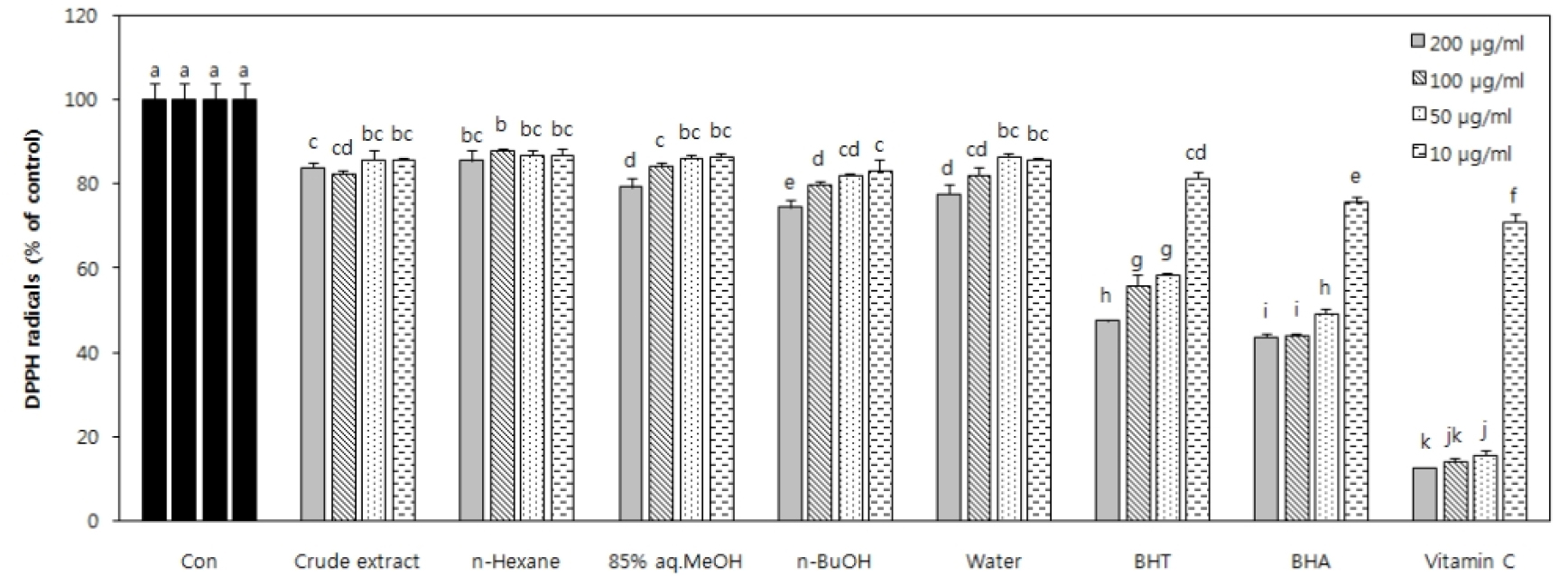
Fig. 2.
DPPH radical scavenging activity of crude extract and its solvent fractions of C. falcatum. 85% aq.MeOH: 85% aqueous methanol, n-BuOH: n-butanol, BHA: butylated hydroxyanisole. a–kMeans with different letters at the same concentration are significantly different (p < 0.05) by Duncan’s multiple range test
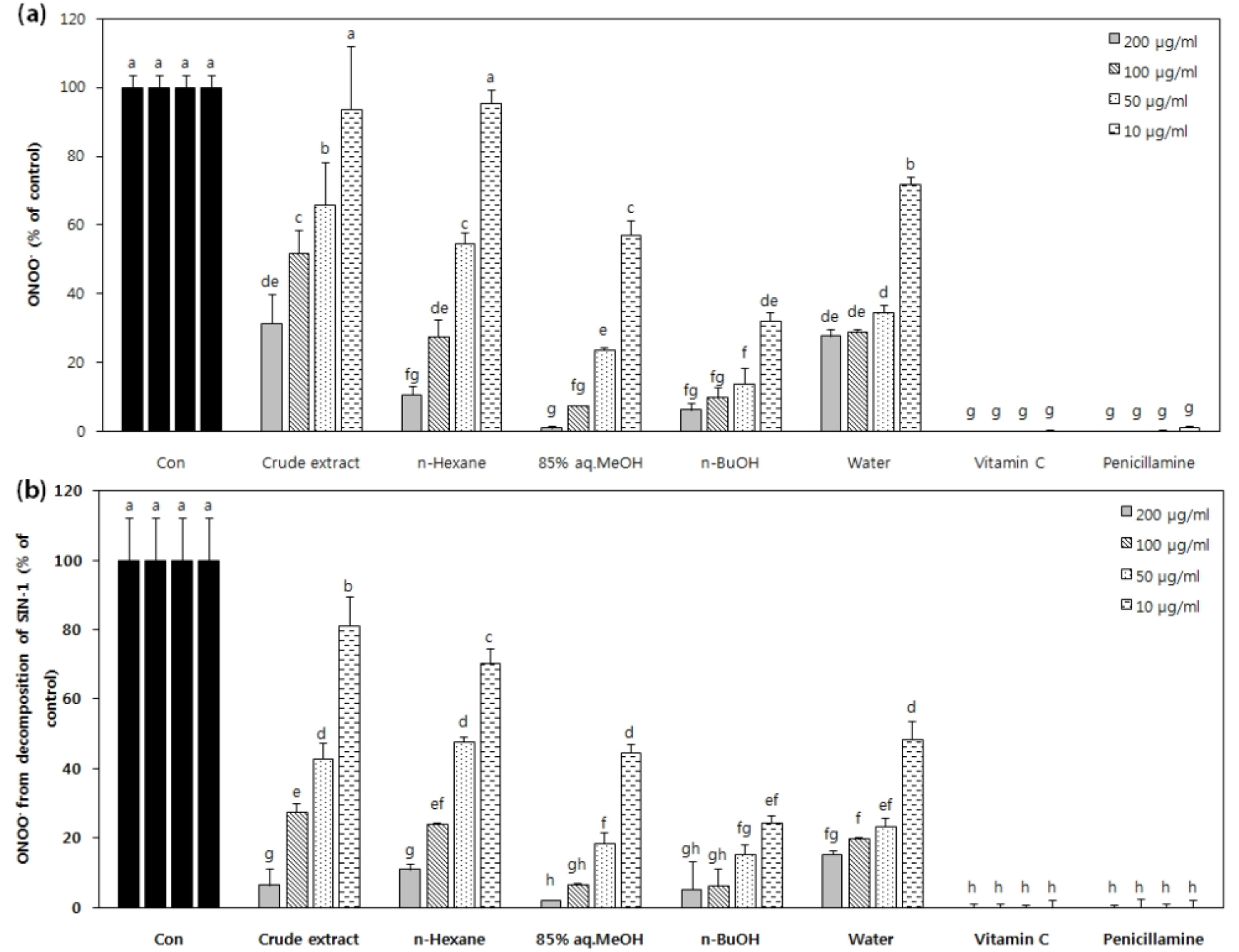
Peroxynitrite 소거 활성
도깨비고비의 추출물 및 용매 분획물의 peroxynitrite 소거 활성을 측정하였다. Rhodamine 123에 ONOO-와 SIN -1을 처리하였고, 그 반응 생성물의 흡광도를 측정하여 나타내었다. 비교하기 위한 대조군으로는 vitamin C와 penicillamine을 사용하였고, 추출물 및 분획 층과 대조군 모두 200, 100, 50 및 10 μg/ml의 농도를 사용하여 결과를 측정하였다. 실험 결과 물 층을 제외한 모든 용매 분획 층이 200 μg/ml 농도에서 20% 이하의 ONOO- 측정값을 보여 유의적인 소거활성을 가진다고 볼 수 있었고, 특히 85% aq.MeOH과 n-BuOH 분획 층에서 각각 200 μg/ml 농도에서 1.0%, 6.3%의 ONOO- 함량을 보였다(Fig 3a). SIN-1의 실험결과도 마찬가지로 ONOO- 측정 실험과 유사한 양상을 보였으며, 특히 85% aq.MeOH과 n-BuOH의 200 μg/ml 농도에서 2.0, 5.2%의 SIN-1 함량을 보여 높은 항산화 활성을 나타내었다(Fig 3b).
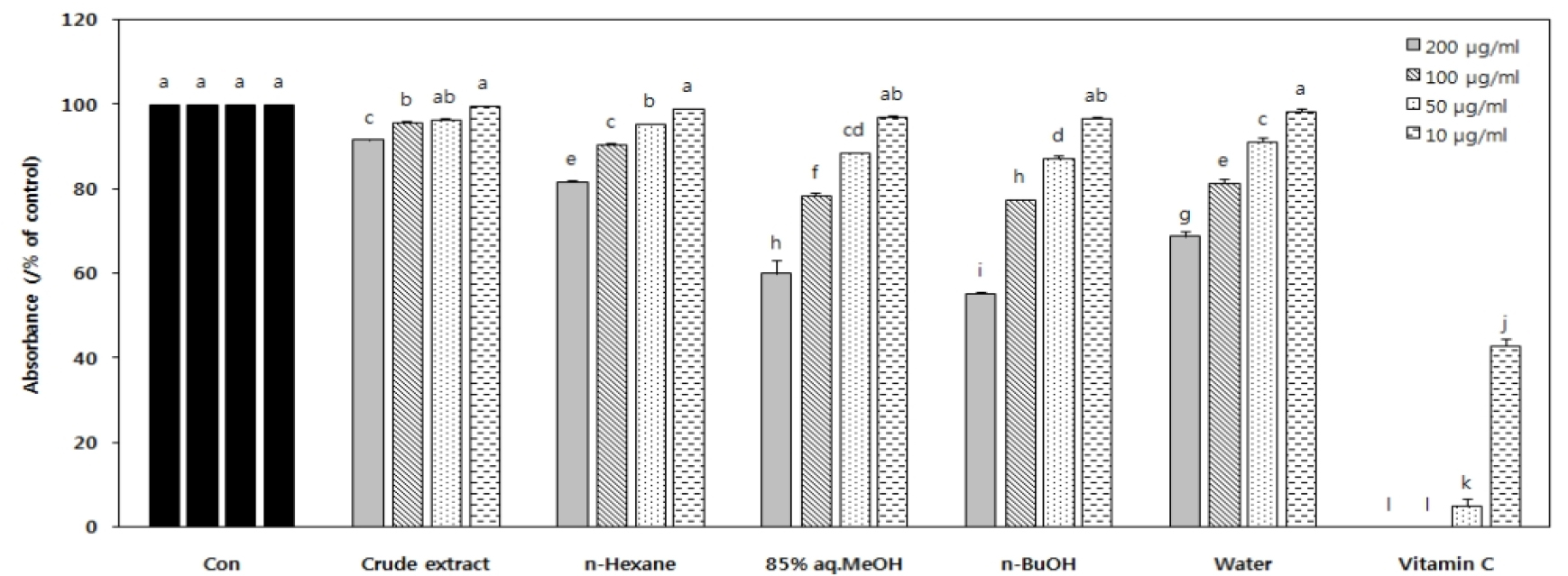
Ferric reducing antioxidant power (FRAP) 측정
FRAP assay를 통하여 도깨비고비의 추출물 및 용매 분획물의 철 환원력을 알아보았다. DPPH, peroxynitrite 실험과 마찬가지로 샘플 각각의 농도는 200, 100, 50 및 10 μg/ml의 농도로 실험을 진행하였고, 대조군으로는 시료를 처리하지 않은 control을 100%로 두고 각각의 시료들의 환원력을 상대적인 % 값으로 표시하였으며 비교하기 위하여 vitamin C의 환원력도 같이 측정하였다. 모든 용매분획물들이 유의적인 환원력을 나타내었으나 85% aq.MeOH와 n-BuOH 분획물들이 200 μg/ml의 농도에서 각각 40.0, 44.6%의 비교적 좋은 환원력을 나타내었다(Fig. 4).
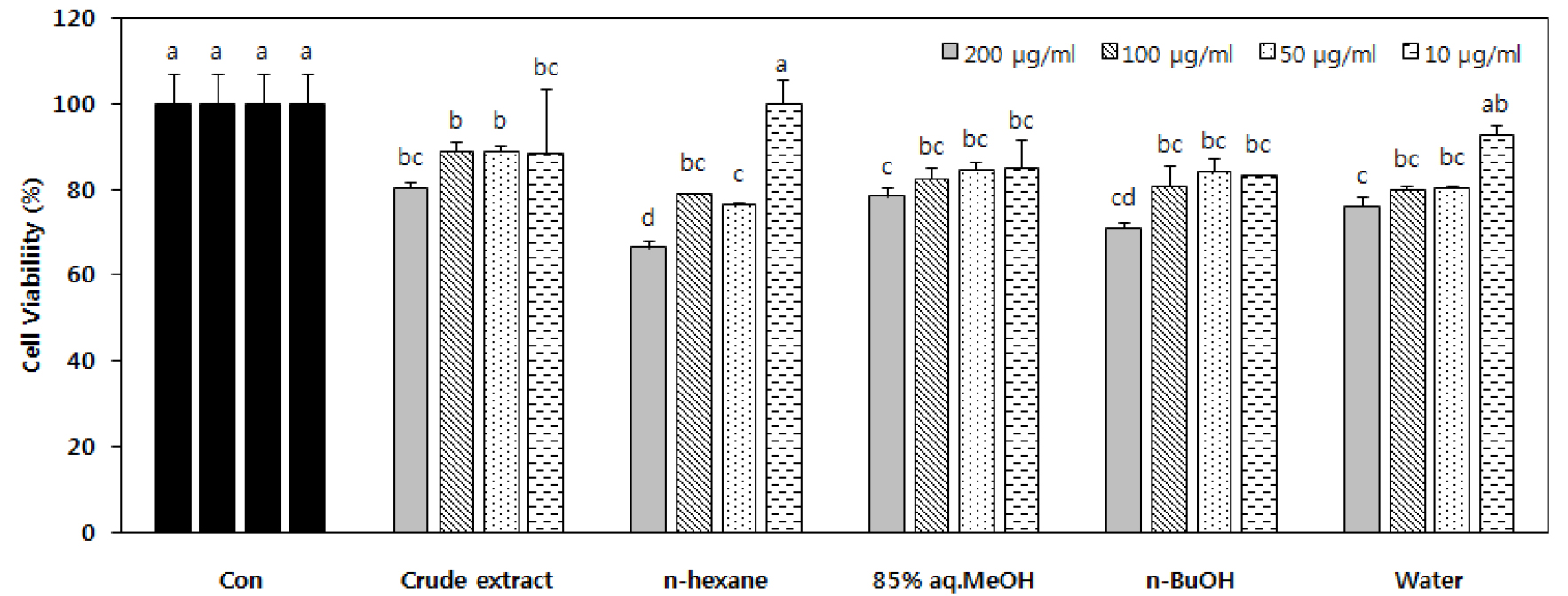
세포내 ROS 소거 활성
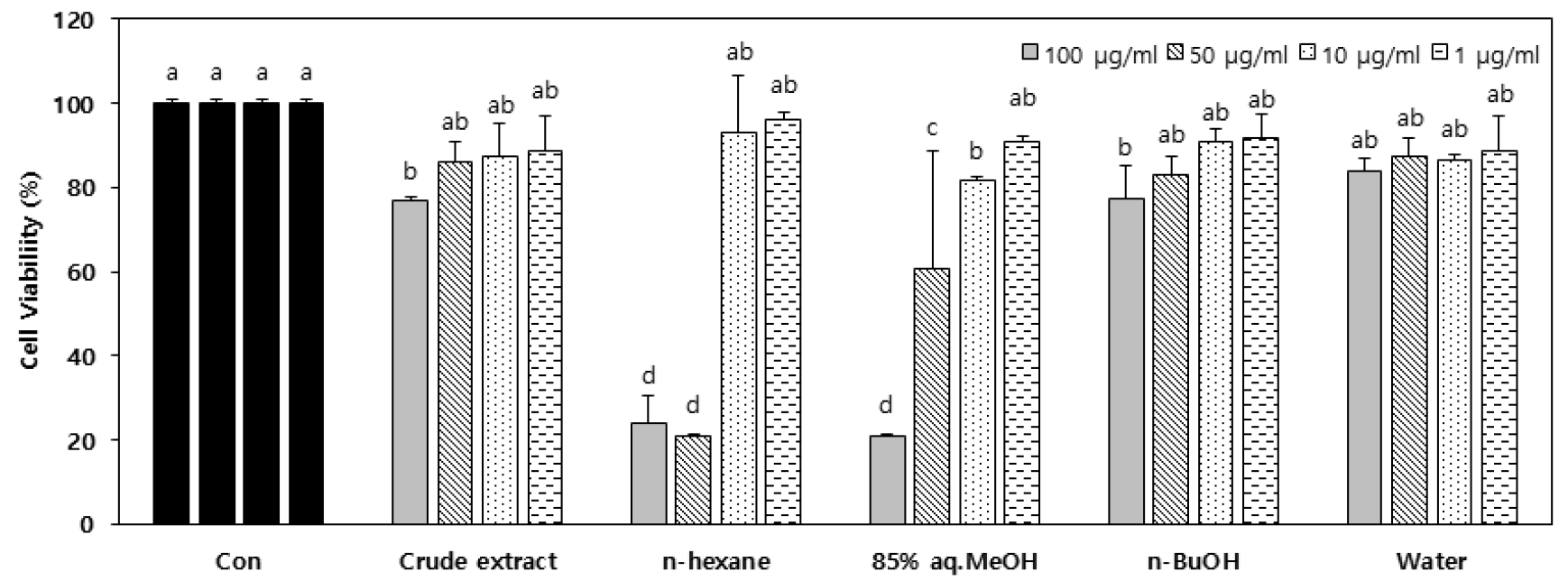
세포주를 활용한 항산화 실험을 진행하기에 앞서 도깨비고비의 추출물 및 용매 분획물의 세포독성을 MTT assay를 통해 HT-1080 세포주에서 확인하였다. 추출물을 포함하여 모든 실험군이 200 μg/ml의 농도에서 80% 이하의 생존율을 나타내어 200 μg/ml의 농도는 제외하였으며, 100 μg/ml이하의 농도에서는 n-hexane 층을 제외한 모든 실험군이 80%이상의 생존율을 보여 주었고, n-hexane 층도 100 μg/ml 농도에서 79.1%의 생존율을 보였기에, 세포주를 활용한 항산화 활성실험은 100 μg/ml를 최고농도로 하여 실험을 진행하였다(Fig. 5).
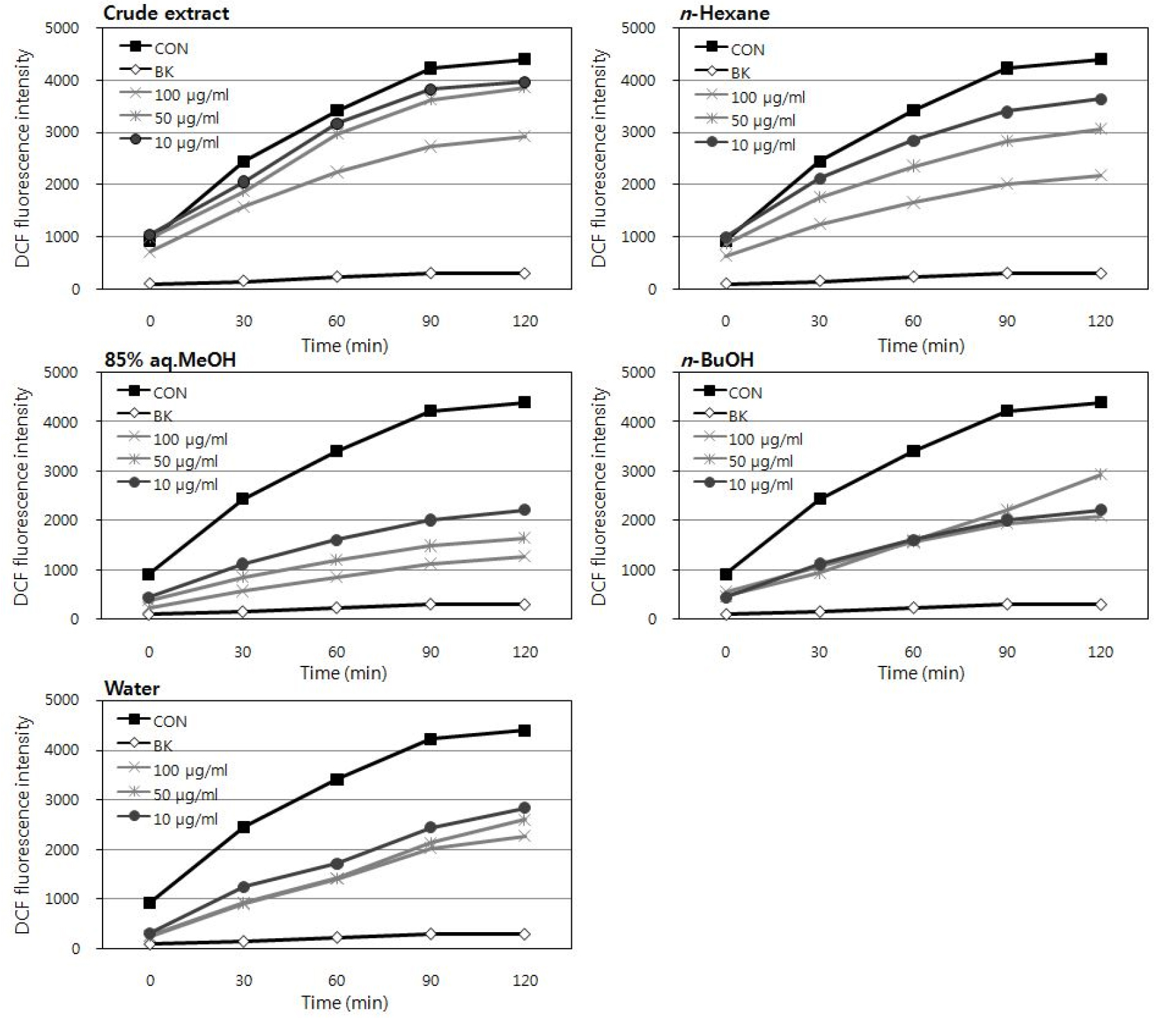
세포내 활성산소종 소거활성을 알아보기 위해 HT-1080 세포주를 활용하여 실험을 진행하였다. H2O2 처리 후 0분부터 30분 간격으로 120분까지 총 5 번에 걸쳐 흡광도를 측정하였고, H2O2로 처리한 control의 흡광도를 가장 높게, H2O2로 처리하지 않은 blank의 흡광도가 가장 낮게 나타나게 설계하였다. 실험 결과 각 용매 분획물의 100 μg/ml 농도에서 control과 blank의 흡광도 차이를 100%로 설정하였을 때 모든 용매 분획물이 50% 이하의 흡광도를 나타내었고, 이 중에서 85% aq.MeOH 분획물이 22.7%로 가장 낮은 흡광도를 나타내어 가장 높은 소거활성을 보여주었다(Fig. 6).
Genomic DNA의 산화억제 활성 측정
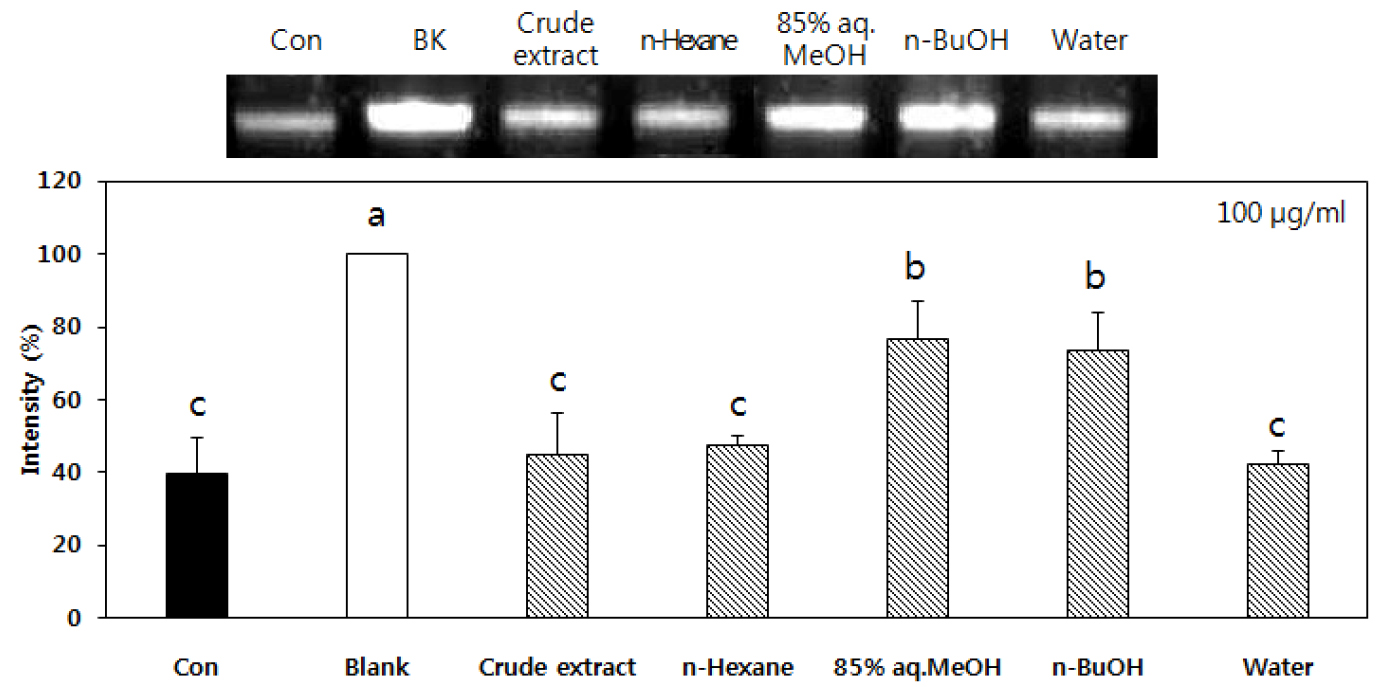
HT-1080 세포로부터 추출한 genomic DNA에 대한 도깨비고비 추출물 및 용매 분획물의 항산화능력을 측정하였다. 추출한 DNA에 도깨비고비 추출물 및 용매 분획물을 처리하고 H2O2와 FeSO4로 산화시켜 샘플이 얼마나 DNA의 산화를 방지하는지 측정하였다. 샘플로 처리하지 않아 가장 산화가 많이 되는 control과 산화제를 처리하지 않아 산화가 되지 않는 blank를 사용하여 값을 비교하였다. 85% aq.MeOH 층과 n-BuOH 층에서 가장 많이 산화를 방지하였으며 blank의 intensity를 100%로 하였을 때 각각 77.0, 73.7%의 intensity를 나타내어 좋은 산화 억제 활성을 보였다(Fig. 7).
총 폴리페놀과 총 플라보노이드 함량 분석
도깨비고비의 추출물 및 용매 분획물의 항산화 구성성분을 확인하기 위하여 총 폴리페놀함량을 측정하였으며 그 결과는 Table 1과 같다. 폴리페놀 화합물은 식물계에서는 널리 분포하고 있는 화합물로서, 두 개 이상의 phenolic hydroxy 작용기를 갖는 방향족 화합물이며(Yu et al. 2006), 단백질 등 여러 화합물과 쉽게 결합하는 특성을 가지고 있어 항산화, 항암 및 항염증 등의 효과가 우수한 것으로 보고되어 있는 화합물이다(Kalt et al. 2010).
Table 1.
Total polyphenol and total flavonoid contents of crude extract and its solvent fractions of C. falcatum. a–cMeans with different letters at the same concentration are significantly different (p < 0.05) by Duncan’s multiple range test
도깨비고비의 85% aq.MeOH 층에서 55.50 mg/g, n- BuOH 층에서 81.50 mg/g의 polyphenol 함량을 나타내었다. 총 flavonoid 함량에서도 polyphenol 함량과 마찬가지로 85% aq.MeOH 층과 n-BuOH 층에서 각각 42.34 mg/g, 56.30 mg/g의 함량을 나타내었다(Table 1). Polyphenol과 flavonoid를 다량 함유하고 있다고 알려진 과일인 블루베리의 경우 70% aq.MeOH 추출물에서 42.26 mg/g의 polyphenol 함량과 26.39 mg/g의 flavonoid 함량을 보인 연구결과가 있으며(Chung 2014), 이와 비교하였을 때도 도깨비고비의 85% aq.MeOH 분획층과 n-BuOH 분획 층은 polyphenol과 flavonoid 함량이 높게 측정되었기에 이 두 분획물의 항산화 활성이 높게 나타난 것은 적어도 부분적으로는 여기에서 기인된 것으로 추측된다.
NO 생성 억제능 측정
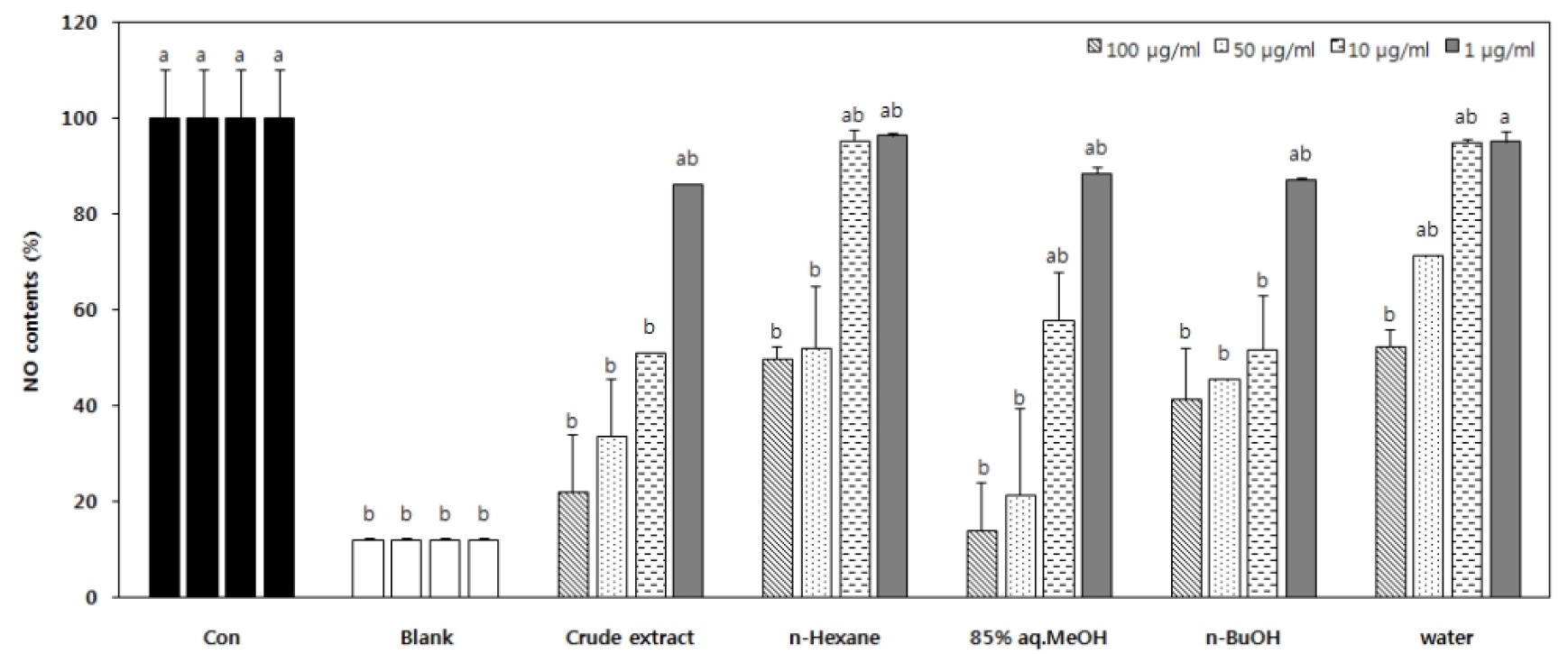
Griess 시약은 세포 내 생성된 아질산염과 반응하여 분홍색의 아조염을 형성하고 이 아조염의 농도는 NO의 농도와 일치하기 때문에 이 원리를 이용하여 NO의 함량을 측정하였다. 실험 결과 85% aq.MeOH 층에서 가장 높은 활성을 나타내었으며, control의 값을 100%로 설정하였을 때, 85% aq.MeOH 층의 100 μg/ml 농도에서 blank값인 12.1%에 근접한 14.2%의 NO 함량을 보였으나 85% aq.MeOH 분획층이 50 μg/ml 이상의 농도에서 Raw 264.7 세포가 60% 이하의 생존율을 보였기 때문에 세포독성에 의한 효과가 큰 영향을 미친 것으로 여겨졌다. 하지만 세포독성을 나타내지 않았던 10 μg/ml의 농도에서 57.8%의 NO 함량을 나타내어 85% aq.MeOH 분획층이 유의적인 NO 생성억제 효과가 있음을 보여 주었다(Fig. 8). 100 μg/ml 이하의 농도에서 독성을 나타내지 않았던 n-BuOH 분획에서는 100 μg/ml 뿐만 아니라 10 μg/ml의 농도에서도 51.9%의 NO 함량을 보여 주어 상당히 좋은 NO 생성억제 효과를 나타내었었다. 전체적으로는 측정농도에서 세포독성을 보이지 않았던 조추출물이 농도의존적으로 가장 좋은 NO 생성 억제효과를 보여 주었으며 100 μg/ml의 농도에서 22.1%의 NO 함량을 나타내었다(Figs. 8 and 9).
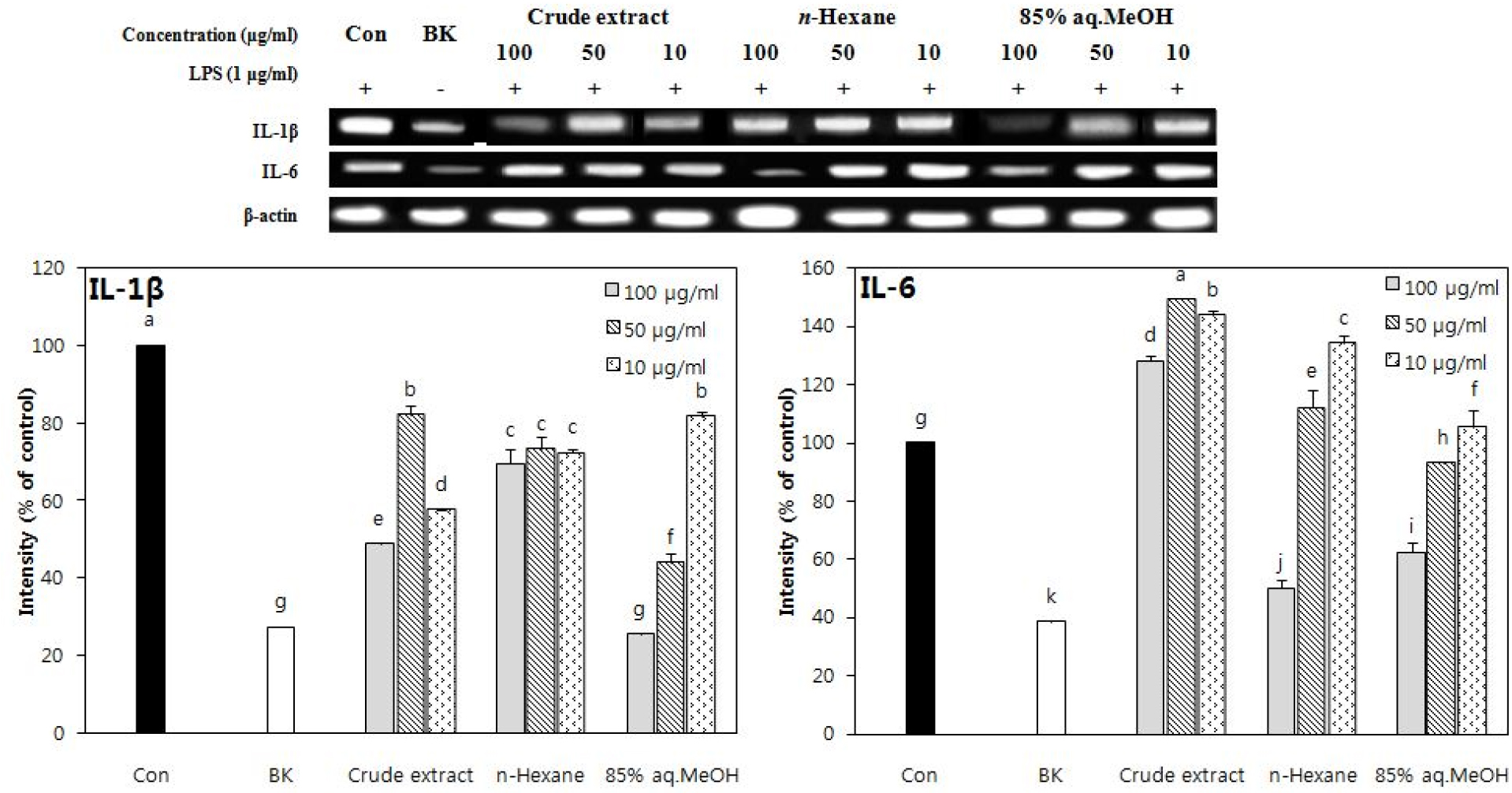
IL-1β, IL-6 및 COX-2의 mRNA 유전자 발현 저해효과
IL-1β와 IL-6 등과 같은 유전자는 활성화된 대식세포에서 과하게 생성되어 발열이나 조직손상 등의 염증반응을 촉진하는 염증성 사이토카인(cytokine)으로 잘 알려진 인자로서, 정상조직에서 발현될 뿐만 아니라 병변 과정에서 그 발현 정도가 증가되며, 인간의 염증성 피부질환과 관련이 있는 것으로 보고되어 왔다. 또 COX-2는 염증부위에서 발현되며 면역세포의 활성을 유도하여 염증매개체인 PGE2라는 염증 매개체를 생합성하는 것으로 알려진 인자이다. PGE2는 통증, 발열 등 염증반응과 면역반응에 관여하고 혈관신생을 촉진시키는 것으로 알려져 있다.
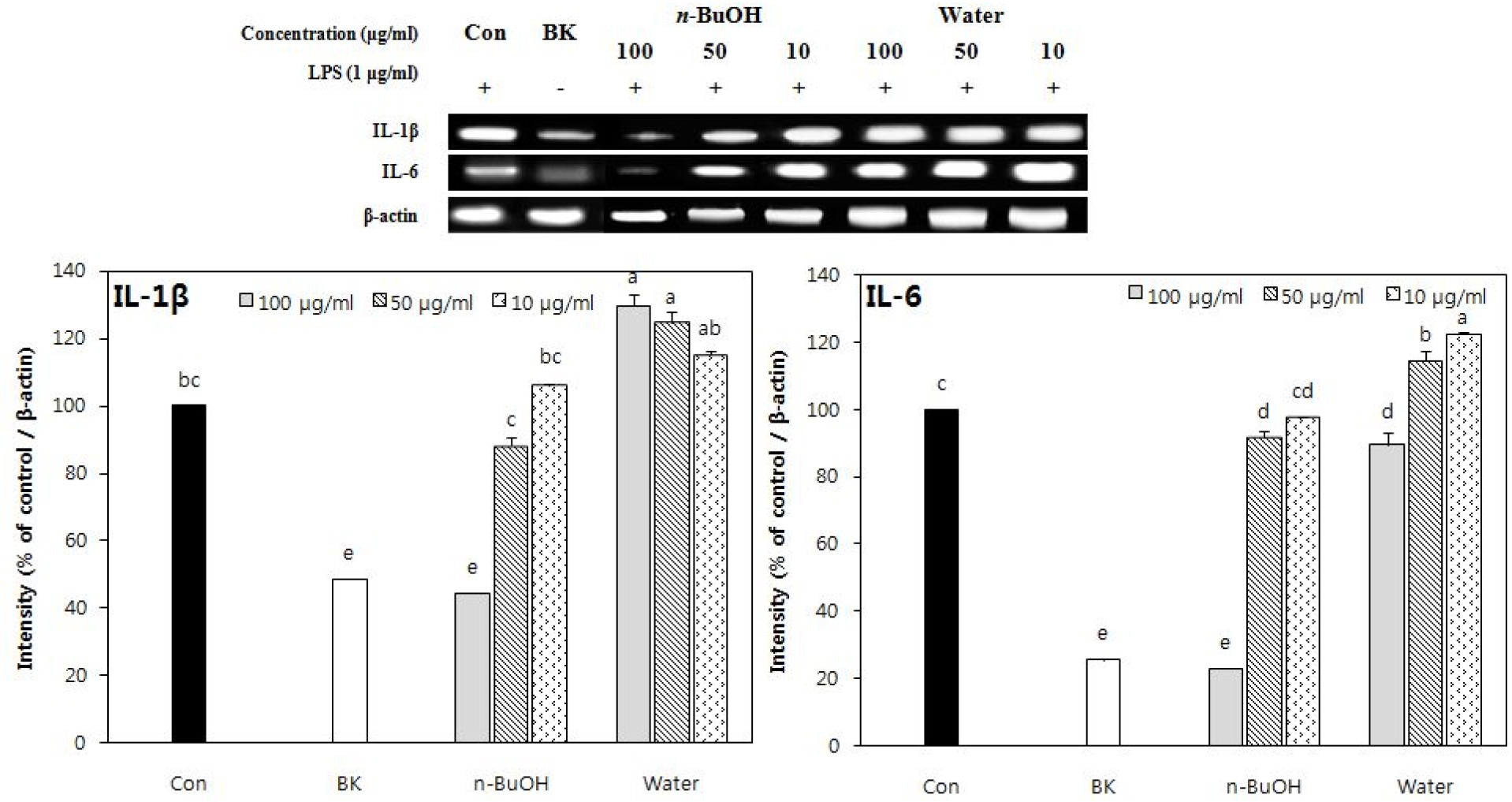
먼저 IL-1β의 경우에는 85% aq.MeOH 분획 층과 n- BuOH 분획층이 100 μg/ml 농도에서 mRNA가 각각 25.8%,44.4%의 발현을 보였으며, 이는 시료로 처리하지 않은 blank의 발현(각각 27.5%, 48.6%) 보다도 낮은 발현도를 나타내었다. IL-6의 발현에서는 IL-1β의 발현을 억제하였던 85% aq.MeOH 분획층과 n-BuOH 분획층이 100 μg/ml 농도에서 각각 62.4%, 23.0%의 발현도를 나타내었다(blank의 발현도는 각각 38.7%, 25.6%). 하지만 이와 같은 85% aq.MeOH 분획층에 의한 IL-1β와 IL-6의 낮은 발현도는 50 μg/ml 이상의 농도에서 나타난 세포독성에 의해 크게 기인된 것으로 여겨 진다(Figs. 10 and 11). n- Hexane 분획층에서도 100 μg/ml 농도에서 IL-6가 낮은 발현도(50.4%)를 보였으나, 50 μg/ml 농도에서는 control 값보다도 높은 발현도(111.9%)를 보였기에 100 μg/ml 농도에서는 세포독성에 기인한 발현도로 유추하였다(Figs. 8 and 10).
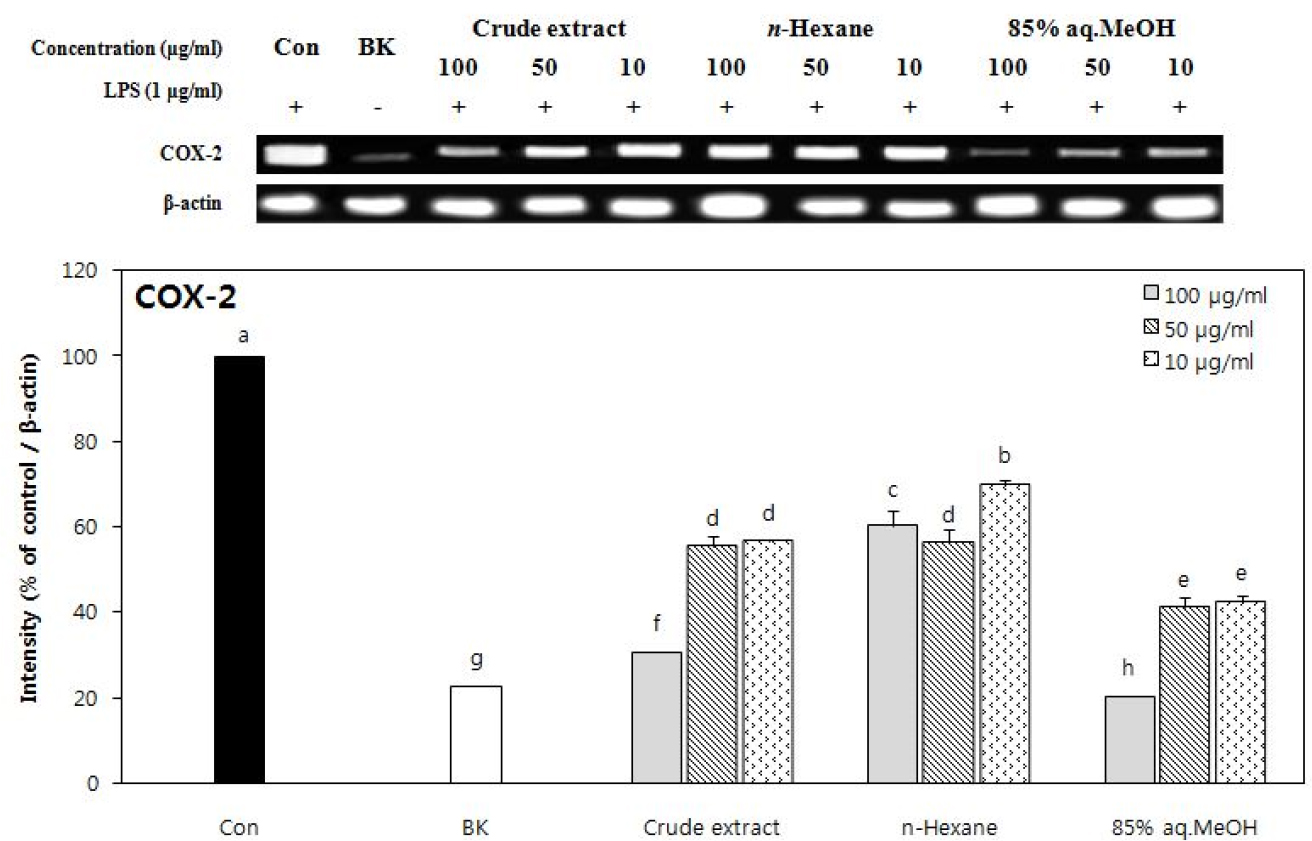
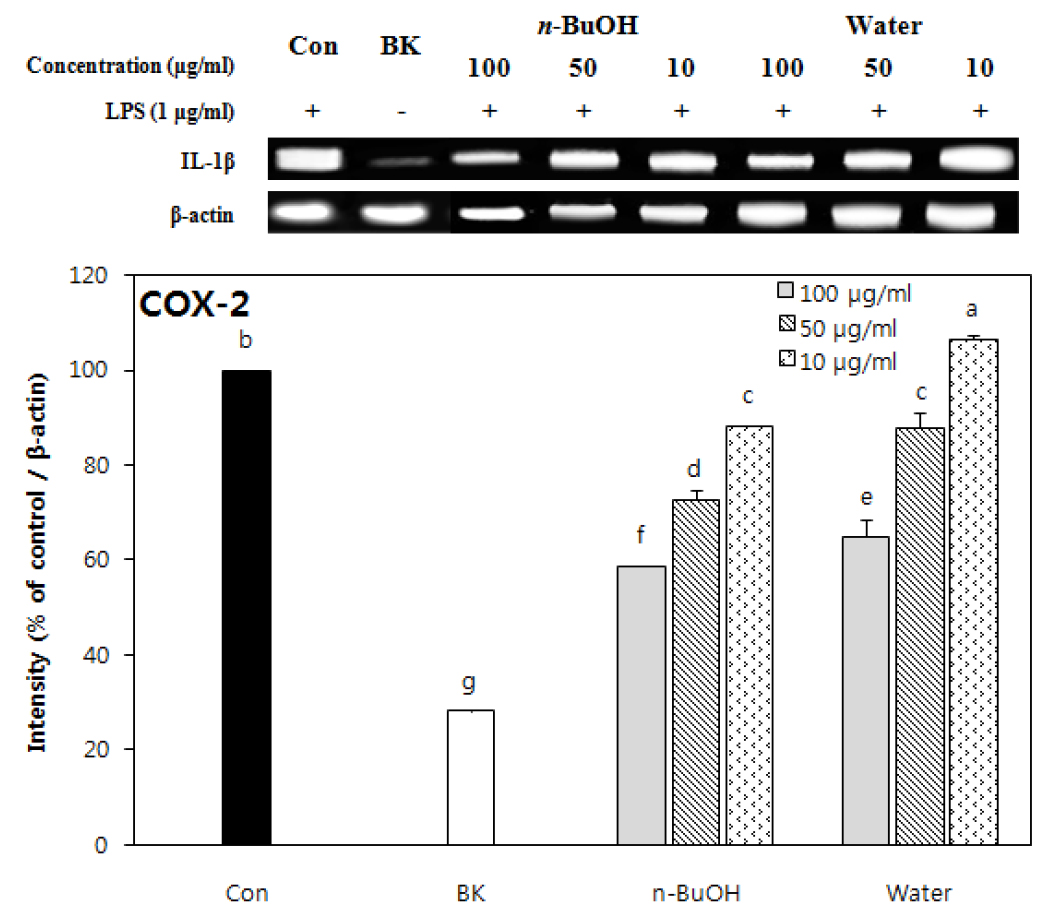
COX-2의 경우에는 100 μg/ml 농도에서 IL-1β와 IL-6의 발현 억제 효과를 나타내었던 n-BuOH 분획층이 유의적인 발현 억제 활성을 나타내지 못했으나, 85% aq. MeOH 층의 100 μg/ml 농도에서는 blank의 발현(22.7%)보다도 낮은 20.3%의 발현을 보였다(Figs. 12 and 13). 그러나 이미 언급한 것처럼 85% aq.MeOH 분획에 의한 발현의 저해는 상당 부분 50 μg/ml이상의 농도에서 나타난 세포독성에 의해 기인된 것으로 여겨진다. 하지만 세포독성을 나타내지 않았던 10 μg/ml의 농도에서 약 42.7%의 발현도를 나타내어 85% aq.MeOH 분획층이 상당한 발현 저해효과가 있음을 보여 주었다. 조추출물도 COX-2에 대한 유의적인 억제활성을 나타내었다.
4. 결 론
Cyrtomium속은 면마(Dryopteridaceae)과에 속하는 양치식물로 35종이 알려져 있으나 C. fortumei(쇠고비)와 C. Caryotideum의 화학적 구성성분과 그 외 수 종의 Cyrtomium속하는 종들의 플라보노이드 성분들에 대한 연구가 보고되었다(Yang et al. 2013b; Iwashina et al. 2006)생리활성으로는 C. macrophyllum의 면역증강 효과, C. Caryotideum의 해열 및 항진균 효과, 그리고 C. fortunei의 멜라닌 생성억제 및 암세포 증식억제 등에 대한 수 편의 논문이 발표된 바 있다(Ren et al. 2014a, 2014b; Ullah et al. 2018; Choi 2013; Yang et al. 2015). Cyrtomium속에 속하는 양치식물들의 항산화 활성에 대해서는 C. fortumei 추출물의 DPPH와 ABTS 라디칼 소거효과 및 지질산화 억제효과, 그리고 C. hookerianum 추출물의 DPPH 라디칼 소거효과가 보고된 바 있다(Jeong et al. 2007; Ding et al. 2008; Yang et al. 2013a). 하지만 도깨비고비의 항산화 및 항염증 활성에 대해서는 전혀 보고되지 않았다.
도깨비고비의 추출물 및 용매 분획물을 이용하여 DPPH radical과 peroxynitrite 소거활성, FRAP, 세포내 ROS 소거활성, 그리고 DNA 산화억제 활성을 측정하였다. DPPH radical에 대해서는 모든 용매 분획 층이 유의적인 소거효과를 나타내지는 않았지만, authentic peroxynitrite와 SIN -1에서 유도된 peroxynitrite에 대해서는 85% aq.MeOH과 n-BuOH 분획 층들이 200 μg/ml의 농도에서 peroxynitrite에 대해서 매우 높은 소거효과를 보여 주었다. FRAP에 대해서는 200 μg/ml의 농도에서 대조군으로 쓰인 vitamin C의 흡광도를 100%로 기준하였을 때, 모든 분획 층이 50% 이상의 활성을 보이지는 못하였으나, 그 중 85% aq.MeOH과 n-BuOH 분획 층은 각각 40.8, 45.4%의 환원력을 보여 주었다. 세포내 ROS 소거활성을 알아본 결과 control과 blank의 차이를 100%로 설정하였을 때, 100 μg/ml 농도에서 85% aq.MeOH 층이 22.7%의 흡광도를 보여 가장 높은 소거활성을 나타내었다. 도깨비고비가 직접적으로 genomic DNA의 산화를 방지하는 정도를 파악하기 위하여 genomic DNA 산화 정도를 전기영동을 통하여 측정하였다. Blank의 intensity를 100%로 설정하였을 때, 85% aq.MeOH 층과 n-BuOH 층의 100 μg/ml 농도에서 각각 77.0, 73.7%의 intensity를 보였다.
세포내 염증반응과 관련된 NO 생성 억제효과에 대해서는 측정농도에서 85% aq.MeOH과 n-hexane 분획층의 세포독성 효과를 고려할 때 n-BuOH 분획층이 용매분획들중에서는 가장 좋은 효과를 나타내었으며 전체적으로는 조추출물이 좋은 효과를 나타내었다. PCR 기법을 사용하여 염증성 인자들인 IL-1β, IL-6 및 COX-2의 mRNA 발현에 대한 측정에서는 세포독성을 보이지 않았던 n-BuOH 분획층이 100 μg/ml 농도에서 IL-1β와 IL-6에 대해서 blank 보다도 낮은 발현도를 나타내었다.
도깨비고비 추출물은 또한 종양괴사인자 알파(TNF-α)도 농도의존적으로 억제하는 것으로 나타났다. TNF-α는 면역반응에 중추적인 역할을 하는 사이토카인(cytokine)이다. 인터루킨-1(IL-1), 인터루킨-6(IL-6) 등과 함께 전신 수준에서 일어나는 면역반응을 관장하며 TNF-α의 이상 발현은 알츠하이머병, 자가 면역질환, 패혈증 등 여러 질환과 관련되어 있다. TNF-α를 억제하면 아랫단계에서 염증반응, 염증 유전자 발현조절 등이 가능하다. 따라서 도깨비고비 추출물은 복합적인 메커니즘으로 염증을 억제할 수 있다.
도깨비고비의 항산화 활성성분의 종류를 확인하기 위하여 폴리페놀과 플라보노이드의 함량을 측정한 결과 85% aq.MeOH 층과 n-BuOH 층이 각각 55.50, 81.50 mg/g의 총 폴리페놀 함량과 42.34, 56.30 mg/g의 총 플라보노이드 함량을 보였다. 문헌조사결과 도깨비고비로부터 플라보노이드 유도체들인 quercetin 3-O-glucoside, kaempferol 3-O-glucoside, kaempferol 7-O-(6″-succinyl)-glucoside, vitexin, orientin, cyrtopterinetin 그리고 cyrtominetin이 분리 보고되었다(Iwashina et al. 2006).
본 연구에서 진행한 모든 항산화 활성실험 결과 85% aq.MeOH 분획 층이 대체적으로 가장 항산화 능력이 높았고, n-BuOH 분획 층의 항산화 활성도 높게 측정이 되었다. 이는 용매 분획 층이 보유한 polyphenol의 역할로 추정이 되나, 폴리페놀 함량이 더 높았던 n-BuOH 분획 층이 85% aq.MeOH 분획층보다 활성이 떨어지는 것으로 보아 폴리페놀 이외에도 항산화 활성을 보이는 구성성분들이 85% aq.MeOH 분획 층에 함유되어 있는 것으로 추정되었으며 현재 좋은 항산화와 항염증 효과를 보였던 85% aq.MeOH, n-BuOH 분획 층에서 항산화 및 항염증 물질을 분리하기 위한 연구가 진행 중에 있다.